Therapeutische conferentie voor de ziekte van Huntington 2021 - dag 3
Updates van dag 3 van de 2021 CHDI therapeutische conferentie over de ziekte van Huntington #HDTC2021


 Geschreven door Dr Rachel Harding, Dr Leora Fox en Professor Ed Wild 25 juni 2021 Bewerkt door Dr Rachel Harding Vertaald door Gerda De Coster Origineel gepubliceerd op 29 april 2021
Geschreven door Dr Rachel Harding, Dr Leora Fox en Professor Ed Wild 25 juni 2021 Bewerkt door Dr Rachel Harding Vertaald door Gerda De Coster Origineel gepubliceerd op 29 april 2021
We zijn terug voor de laatste dag van de virtuele 2021 CHDI Therapeutics conferentie. Dit artikel vat onze live Twitter-updates samen over de spannende wetenschap die wordt gepresenteerd. Je kunt deze vinden met de hashtag #HDTC2021. De laatste sessie van de conferentie zal het meest recente nieuws geven over meer klinische programma’s voor de ZvH.
Een nieuwe manier om de verschillende stadia van de ZvH te definiëren
De eerste presentatie van de dag was van Sarah Tabrizi en Jeff Long die het HD Integrated Staging System (HD-ISS) voorstelden. HD-ISS heeft tot doel de verschillende stadia van de ZvH opnieuw te definiëren om alle complexiteit en variabiliteit van de ziekteprogressie te omvatten.
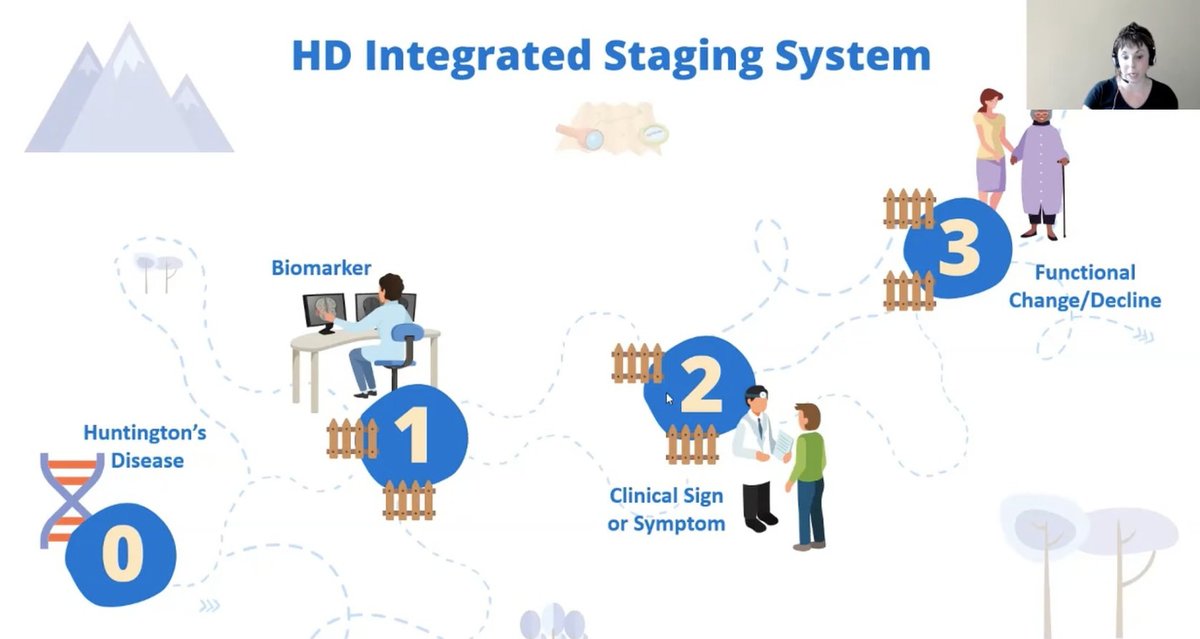
Het nieuwe systeem is het resultaat van veel en hard werk van het HD Regulatory Science consortium, een wereldwijd netwerk van academici, industriewetenschappers en experts op het gebied van geneesmiddelenregulering. De HD-RSC bestaat om een raamwerk op te zetten waarmee goede medicijnen voor de ZvH probleemloos kunnen worden getest en goedgekeurd.
Het belangrijkste doel van HD-ISS is om klinische proeven mogelijk te maken bij mensen voordat ze bewegingsproblemen ontwikkelen door de ZvH (motorische diagnose). Deze onderzoeken zijn bedoeld om het begin van de ziekte te voorkomen of uit te stellen. Tabrizi wees erop dat het HD-ISS-raamwerk geen poging is om klinisch-diagnostische of ziektefase-criteria opnieuw uit te vinden. Het is puur een onderzoeksinstrument om selectie en monitoring van patiënten voor klinische proeven mogelijk te maken, een belangrijk onderscheid.
Actuele onderzoeken definiëren ziektefases op basis van ‘mijlpalen’ met afkapwaarden. De meest duidelijke afkapwaarde bij de ZvH is het concept van ‘motorische diagnose’. Deze werd gebruikt om de ziekte te diagnosticeren, zelfs voordat we de genetische oorzaak kenden. Maar biologisch gezien weten we nu dat de ZvH een continuüm is. Ze ontwikkelt zich langzaam, beïnvloedt mensen heel anders en heeft een lange periode waarin mensen zich normaal voelen en er normaal uitzien, maar we kunnen met bloedonderzoek en scans zien dat de mutatie al enig effect heeft op de hersenen.
Voor onderzoeksdoeleinden stelt Tabrizi een nieuwe definitie van de ZvH voor. In haar concept kent de ziekte 4 opeenvolgende stappen: de ziekte (het levenslange effect van het gen); detectie van de effecten van het gen (biomerkers); symptomen; en functionele verandering (verlies van het vermogen om dingen te doen).
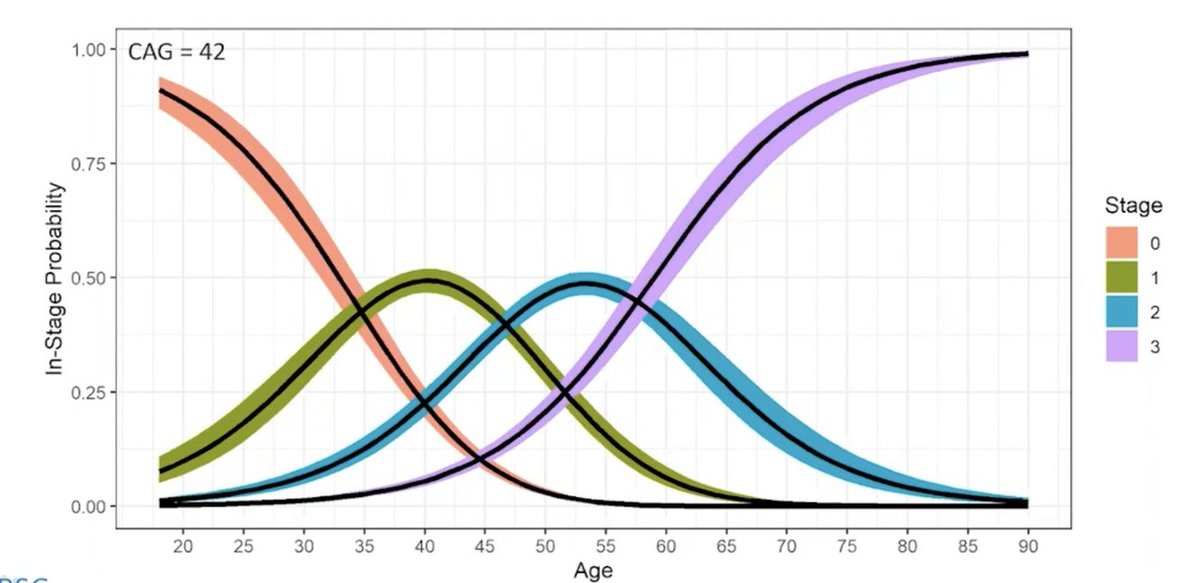
Deze wijzigingen worden benoemd als fasen 0 tot 3 en de overgang van de ene fase naar de andere wordt bepaald door overeengekomen mijlpalen. Jeff Long legde uit dat de afkapwaarde voor elke mijlpaal systematisch werd bepaald met de hulp van grote datasets, bijvoorbeeld door het volume van de caudate in de hersenen te controleren zoals gemeten door MRI. Door middel van cijfers kan Long trajecten uitzetten die laten zien hoe een persoon tijdens zijn leven waarschijnlijk doorheen deze fasen zal evolueren.
Tabrizi legde uit dat dit soort modellering medicijnontwikkelaars in staat stelt onderzoeken te plannen, omdat de terminologie uniform zal worden. Hierdoor ontstaat de mogelijkheid om in te grijpen voordat motorische symptomen zich voordoen. Belangrijk is dat HD-RSC input zocht van niet-wetenschappers (leken) uit huntingtonfamilies via het HD-COPE-netwerk.
Updates over de huntingtine-verlagende proef HD-GeneTRX1 van uniQure
De volgende spreker was David Cooper, die updates gaf over de uniQure huntingtineverlagende gentherapiestudie, waarbij het medicijn AMT-130 werd getest waarover we onlangs schreven.
AMT-130 is de eerste gentherapie voor de ZvH. Het is verpakt in een onschadelijk virus en wordt via een eenmalige operatie in de hersenen afgeleverd. Eenmaal daar zal AMT-130 het recept voor huntingtine-eiwit desactiveren. Cooper vertelde ons over de manier waarop het werd getest bij grote en kleine dieren en hoe aangetoond werd dat het veilig is en goed wordt gedistribueerd naar relevante delen van de hersenen.
Vervolgens introduceerde Cooper de fase I/II-studie, genaamd HD-GeneTRX1. Het gaat om 26 mensen die een van de twee dosissen AMT-130 krijgen of een imitatie-operatie ondergaan. Ze zullen gedurende een jaar nauwlettend worden gevolgd en daarna wat minder frequent gedurende maximaal 5 jaar. Dit is een veiligheidsonderzoek, dus het belangrijkste doel is om te onderzoeken of patiënten geen gevaarlijke bijwerkingen ervaren.
Deelnemers zijn tussen 25 en 65 jaar en hebben vroege huntingtonsymptomen. Ze moeten ook een CAG-herhaling van 44 of meer hebben en voldoen aan andere criteria met betrekking tot de grootte van bepaalde hersengebieden, zodat de procedure veilig kan worden uitgevoerd. De criteria evolueerden een beetje toen ze de patiënten screenden en leerden van de eerste operaties.
Inmiddels zijn 10 patiënten behandeld met een hersenoperatie die wordt uitgevoerd in een MRI. Dit is baanbrekende wetenschap en heeft de neurowetenschappelijke gemeenschap waardevolle lessen opgeleverd dankzij de onbaatzuchtige vrijwilligers in dit onderzoek. Er zijn negen locaties in de VS die patiënten rekruteren en uniQure zal later dit jaar een kleine studie in Europa starten, waarin alle deelnemers het medicijn zullen krijgen (bekend als een open-label onderzoek).
In de vraag en antwoordsessie werd Cooper gevraagd of de resultaten van de Roche-studie de plannen van uniQure voor deze studie veranderden. Hij legde uit dat ze op dit moment verder gaan zoals gepland en dat hun chirurgische leveringsmethode anders is dan die van Roche.
Terugkijken op de gegevens van de SIGNAL-studie
De laatste spreker van de sessie was Maurice Zauderer van Vaccinex. Zauderer presenteerde resultaten van de recente SIGNAL-studie waarin werd gekeken of het medicijn pepinemab tegen de huntingtonsymptomen hielp. We schreven er hier eerder over.
In deze studie kregen ongeveer 250 mensen met vroege huntingtonsymptomen gedurende meer dan een jaar pepinemab via een maandelijkse intraveneuze injectie. Zij werden opgevolgd m.b.t veiligheid en verbetering van symptomen. De focus lag op het meten en observeren van ernstige bijwerkingen en cognitieve- en bewegingssymptomen. Het medicijn was veilig, maar er werd geen algehele verbetering vastgesteld bij patiënten in verschillende cognitieve tests die planning en geheugen beoordelen.
Toen Zauderer en collega’s de gegevens onderzochten, zagen ze enkele kleine voordelen van de behandeling bij een subgroep patiënten die vroege tekenen van symptomen vertoonden. Dit was echter niet het geval bij een patiëntengroep die geen symptomen vertoonde.
Het SIGNAL-onderzoek voldeed niet aan het primaire eindpunt en deze bevindingen zijn voortgekomen uit een daaropvolgende analyse van de onderzoeksgegevens. Hoewel dit voordeel bij mensen met vroege huntingtonsymptomen potentieel goed nieuws is, zou dit verder moeten worden onderzocht.
Naar een betere samenwerking in de huntington-onderzoeksgemeenschap
De laatste spreker van de conferentie was Aled Edwards van het Structural Genomics Consortium. Hij sprak over een manier om de wetenschappelijke huntingtongemeenschap en onderzoekers uit de industrie in het bijzonder beter te laten samenwerken op het gebied van de ontdekking van geneesmiddelen, de identificatie van genen en manieren om deze te behandelen met therapieën. Het ontdekken van medicijnen begint vaak met een enorm scala aan mogelijkheden die in de loop van de tijd worden verkleind naarmate onderzoek meer onthult over de biologie van de ZvH.
Edwards is een groot voorstander van open wetenschap en het delen van gegevens. Hij suggereerde dat de vermeende juridische en financiële belemmeringen om dit te doen, zelfs binnen de privé-sector, gemakkelijk kunnen worden overwonnen en mensen met de ZvH en vele andere ziekten ten goede kunnen komen. De huntingtongemeenschap werkt al zo nauw samen dat het mogelijk de lat voor anderen zou kunnen leggen door enkele van deze strategieën te implementeren. Uitstekende stof tot nadenken aan het einde van drie volle dagen van delen van informatie over het meest recente huntingtononderzoek onder academici, clinici en leden van de industrie.
Al uitkijken naar HDTC 2022!
En dat is alles mensen! We hopen dat dit voor iedereen een nuttige manier is geweest om het laatste nieuws te leren over het zoeken naar medicijnen voor de behandeling van de ZvH.


