
Lancering: Eerste mensen behandeld met gen-onderdrukkende medicijnen voor ZvH!
Belangrijke Aankondiging: Eerste ZvH-patiënten behandeld met gen-onderdrukkende medicijnen

Vandaag komt het nieuws dat de eerste Ziekte van Huntington-patiënten succesvol zijn behandeld met gen-onderdrukkende medicijnen gericht op het HD-gen. Deze moedige vrijwilligers zijn de eerste ZvH-patiënten die ooit zijn behandeld met medicijnen die de ZvH bij de wortel aanpakken, een behandelingsmethode met enorm potentieel. Waarom zijn we zo enthousiast over dit nieuws?
Gen-onderdrukking
Veel ZvH-onderzoekers, waaronder de redacteuren van HDBuzz, geloven dat een behandelingsmethode genaamd gen-onderdrukking momenteel het meest opwindende is wat er in het ZvH-onderzoek gebeurt. Om te begrijpen waarom, moeten we eerst wat basiskennis over ZvH behandelen.
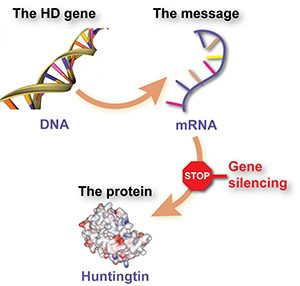
Elke ZvH-patiënt heeft een gemuteerde versie geërfd van een gen dat we soms het HD-gen noemen. In wetenschappelijke kringen wordt het gen eigenlijk Huntingtine genoemd, afgekort als HTT, maar dat kan wat verwarrend zijn.
Iedereen op aarde heeft twee kopieën van het HD-gen, één geërfd van moeder en één van vader. Bij elke ZvH-patiënt heeft een van deze kopieën een soort genetische stottering, een herhalend stukje code bij het uiteinde van het gen dat de werking van dit gen beïnvloedt. Dit blijkt slecht nieuws te zijn – de Ziekte van Huntington ontstaat wanneer deze stottering langer wordt dan een kritieke drempel.
We begrijpen nog steeds veel niet over ZvH. Wat het HD-gen normaal doet, waarom het dit herhalende stuk DNA heeft, en wat ervoor zorgt dat het uitrekt zijn vragen waarover we nog geen wetenschappelijke consensus hebben.
Maar wat absoluut zeker is, is dat elke ZvH-patiënt hetzelfde type mutatie heeft – een verlenging van het herhalende stuk DNA in het HD-gen. In de code die wetenschappers gebruiken om genetische sequenties te beschrijven, worden de stotterende letters afgekort als “C-A-G”, daarom heb je mensen misschien horen praten over “C-A-G herhalingen”.
Deze genetische zekerheid is angstaanjagend voor familieleden – als je moeder of vader ZvH heeft, heb je precies 50% kans om deze vreselijke mutatie te erven. Maar er is een keerzijde aan dit slechte nieuws, namelijk dat deze zekerheid ons een heel goed doelwit geeft om ZvH aan te vallen. Aangezien elke ZvH-patiënt een gemuteerd HD-gen heeft, waarom proberen we niet gewoon van het gemuteerde gen zelf af te komen?
In vorige generaties zou dit zijn alsof je iemand vroeg om naar de hemel te reiken en je favoriete ster te plukken, maar we leven in een geweldige tijd. Het blijkt dat dit soort dingen nu mogelijk zou kunnen zijn omdat wetenschappers in de afgelopen 20-30 jaar technieken hebben ontwikkeld waarmee we een bepaald gen naar wens kunnen uitschakelen.
In essentie zijn wetenschappers een nieuwsgierig volkje. Terwijl ze onderzochten hoe cellen bepaalde taken uitvoeren, hebben ze een breed scala aan manieren ontdekt om bepaalde genen uit te schakelen. Je hoort misschien over “antisense oligonucleotiden (ASO’s)”, of “zinkvinger nucleasen (ZFN’s)” of zelfs “transcriptie activator-achtige effector nucleasen (TALEN’s)”. Het idee achter deze verzameling benaderingen is hetzelfde: cellen voor de gek houden om het HD-gen uit te schakelen en alleen het HD-gen.
“Deze genetische zekerheid is angstaanjagend voor familieleden – als je moeder of vader ZvH heeft, heb je precies 50% kans om deze vreselijke mutatie te erven. Maar er is een keerzijde aan dit slechte nieuws, namelijk dat deze zekerheid ons een heel goed doelwit geeft om ZvH aan te vallen.”
Isis en ASO’s
Een breed scala aan wetenschappers past al deze bovengenoemde benaderingen (en meer!) toe op het probleem van het uitschakelen van het HD-gen. Het meest geavanceerde programma gebruikt een type medicijnen genaamd “antisense oligonucleotiden”, of “ASO’s”. In essentie zijn ASO-medicijnen korte, sterk gemodificeerde stukjes DNA die een cel opdragen om een bepaald gen te vernietigen.
Vergeleken met sommige andere technologieën die genen aan- of uitzetten, bestaan ASO’s al lang. Het bedrijf met het meest geavanceerde HD-gen onderdrukkingsprogramma is Isis Pharmaceuticals, opgericht in 1989. Voor degenen onder ons die zich de val van de Berlijnse Muur herinneren, lijkt 1989 misschien niet zo lang geleden, maar in de biotechnologiewereld is dat een lange tijd.
Het voordeel van al deze ervaring is dat Isis een lange geschiedenis heeft in het toepassen van ASO’s op het gebied van menselijke ziekten. Versies van hun verschillende ASO-medicijnen zijn getest bij duizenden mensen met een breed scala aan gezondheidsproblemen. Ze hebben ook met succes medicijnen laten goedkeuren door regelgevende instanties zoals de FDA, dus ze hebben een realistisch beeld van wat er nodig is om een medicijn bij mensen te krijgen.
Gelukkig voor ons heeft Isis een ASO-medicijn ontwikkeld dat ze “ISIS-HTTRx” noemen, dat gericht is op het onderdrukken van het HD-gen. Dieren die behandeld zijn met de muisversie van dit medicijn laten opmerkelijke en belangrijke verbeteringen zien in ZvH-achtige symptomen, wat veel wetenschappers erg enthousiast maakt.
Het succes van HD-onderdrukkende medicijnen bij muizen is nette wetenschap, maar het daadwerkelijk uitvoeren van een studie voor ZvH-patiënten is een groot en duur probleem. Isis begrijpt dat ze partners nodig hebben met diepe zakken en nog meer ervaring met klinische studies om medicijnen zo snel mogelijk bij patiënten te krijgen. Daarom hebben ze samengewerkt met farmaceutische gigant Roche om ISIS-HTTRx zo snel en bekwaam mogelijk te testen.
De eerste HTTRx-studie

Zoals we onlangs beschreven op HDBuzz (http://en.hdbuzz.net/203), is het goedkeuren van medicijnen een lang en ingewikkeld proces. De eerste stap op weg is wat een Fase 1-studie wordt genoemd. Elke fase 1-studie heeft één essentieel doel: ervoor zorgen dat een experimenteel medicijn veilig is voor mensen. Niet muizen, niet apen, niet ratten, maar mensen.
Vaak worden fase 1-studies uitgevoerd bij gezonde vrijwilligers, maar in dit geval wordt de fase 1-studie van ISIS-HTTRx uitgevoerd bij 36 ZvH-patiënten in Canada, het Verenigd Koninkrijk en Duitsland. Dit lijkt misschien een klein aantal patiënten, maar onthoud dat het doel van deze studie is om de veiligheid vast te stellen, dus we willen een klein aantal vrijwilligers behandelen om te kijken naar eventuele problemen voordat we het medicijn in een grotere groep testen.
Dit geldt vooral voor een medicijn zoals ISIS-HTTRx dat rechtstreeks in de hersenen moet worden toegediend. Na veel experimenten heeft Isis een plan ontwikkeld om ASO’s rechtstreeks in de vloeistof die de hersenen omringt, het
Er is veel voorwerk gedaan bij zowel dieren als mensen om deze toedieningsmethode uit te werken, maar natuurlijk moeten we uiterst voorzichtig zijn wanneer we een experimenteel medicijn in iemands hersenen toedienen. Daarom is er een relatief klein aantal patiënten opgenomen in deze eerste fase 1-studie van ISIS-HTTRx.
Deze kwestie van de verspreiding van het medicijn in de hersenen roept een belangrijke zorg op. De gegevens die tot nu toe door Isis zijn verzameld, suggereren dat het medicijn in veel delen van de hersenen komt, maar niet veel in een deel van de hersenen dat het striatum wordt genoemd.
Dit is jammer, omdat het striatum het meest beschadigde deel van de hersenen is bij ZvH. De hoop is dat het repareren van andere delen van de hersenen met een ASO een groot voordeel kan opleveren voor het striatum – uitzoeken of dit waar is, is een van de doelen van deze studies.
Wat is er gebeurd?
“Gelukkig voor ons heeft Isis een specifiek ASO-medicijn ontwikkeld dat ze “ISIS-HTTRx” noemen, dat gericht is op het onderdrukken van het HD-gen.”
Dus wat is het grote nieuws? Simpel – Isis heeft zojuist aangekondigd dat de eerste patiënten met succes zijn behandeld met ISIS-HTTRx. Professor Sarah Tabrizi, wereldwijd hoofdonderzoeker van de studie aan University College London, heeft gezegd: “Ik ben verheugd dat dit antisense-medicijn nu veilig is toegediend aan de eerste patiënten. Families die getroffen zijn door de ziekte van Huntington hebben decennialang op deze mijlpaal gewacht. Ik kijk ernaar uit om het soepele verloop van deze eerste studie te waarborgen en hopelijk ISIS-HTTRx door te zien gaan naar werkzaamheidstests en licentieverlening”.
Dit betekent dat de studie aan de gang is en dat de eerste vrijwilligers zijn behandeld zonder directe complicaties. Het komende jaar zal een periode zijn van intensieve studie van deze proefvrijwilligers om er zeker van te zijn dat ze geen onverwachte complicaties van de behandeling krijgen. Ze zullen ook worden onderzocht op een reeks metingen of het medicijn al dan niet werkt, wat cruciale informatie zal opleveren voor het plannen van toekomstige ZvH-gen onderdrukkingsstudies.
Waar gaat dit heen?
Deze aankondiging vertegenwoordigt een enorme mijlpaal, maar het is slechts één stap op weg naar het ontwikkelen van een gen-onderdrukkende aanpak voor ZvH. Als deze fase 1-studie succesvol is en het medicijn veilig blijkt te zijn, zal er nog een studie nodig zijn om te bewijzen dat het medicijn invloed heeft op ZvH-symptomen. En onthoud ook dat deze studies experimenten zijn waarvan we de uitkomst niet kennen – het is mogelijk dat het medicijn veilig is, maar niet genoeg impact heeft in de hersenen om ZvH-symptomen significant te beïnvloeden.
Dit klinkt ontmoedigend, maar patiënten en families kunnen worden getroost door de wetenschap dat de planning voor deze volgende studie al aan de gang is. Iedereen die bij dit project betrokken is, wil zo snel mogelijk veilige en effectieve medicijnen voor ZvH in de kliniek.
De aankondiging van vandaag vertegenwoordigt een opmerkelijke stap in de lange strijd tegen ZvH. We voelen grote opwinding, evenals een diep gevoel van dankbaarheid aan de onderzoekers en deelnemers aan deze cruciale studie. Blijf HDBuzz volgen voor meer updates terwijl deze studies vorderen.
Meer informatie
Voor meer informatie over ons openbaarmakingsbeleid, zie onze FAQ…


