Ziekte van Huntington Therapeutische Conferentie 2017 – dag 1
HDBuzz geeft een samenvatting van de jaarlijkse Ziekte van Huntington Therapeutische Conferentie op Malta 2017 – dag 1

Hallo iedereen! Het is de jaarlijkse Ziekte van Huntington Therapeutische Conferentie op Malta. Ongeveer 350 wetenschappers van over de hele wereld die werken aan de ZvH komen hier bijeen om de nieuwste ontwikkelingen in onderzoek te bespreken.
Groot nieuws uit big data
De eerste spreker is Leslie Jones van Cardiff University, die onderzoekt hoe genetica de ZvH beïnvloedt. Jones is geïnteresseerd in de manier waarop genetische variaties ervoor zorgen dat de symptomen van mensen met de ZvH-mutatie eerder of later dan verwacht optreden. Ze maakt deel uit van het “GeM-HD” -consortium van onderzoekers dat een mijlpaalstudie in 2015 heeft gepubliceerd. Genetische variaties die de leeftijd van het ontstaan van de ZvH beïnvloeden, werken op dezelfde manier bij mensen met verschillende vormen van “spinocerebellaire ataxie” (SCA). Net als de ZvH worden sommige vormen van SCA veroorzaakt door een verlengde “C-A-G” -sequentie (in verschillende genen). Deze lange, herhaalde stukken “C-A-G” zijn moeilijk voor cellen om nauwkeurig te kopiëren. Als gevolg hiervan worden lange CAG-herhalingen meestal nog langer, vanwege foutjes tijdens het kopiëren en repareren van DNA. De belangrijkste bevinding van het GeM-HD-onderzoek is dat mutaties in DNA-herstelgenen de leeftijd beïnvloeden waarop ZvH-symptomen optreden. Wetenschappers die werken aan de ZvH moeten plotseling veel leren over het proces van DNA-reparatie!

Davina Hensman Moss (UCL) is een belangrijk lid van de groep die onderzoekt hoe genetische variaties de leeftijd van het begin van de ZvH beïnvloeden. We hebben de neiging om te praten over het “begin” van de ZvH, maar de ontwikkeling van de ZvH-symptomen is een lang en langzaam proces. Moss gebruikt informatie uit de TRACK-HD-studie om te begrijpen hoe deze ontwikkeling gebeurt. Informatie uit de TRACK-HD-studie stelde Moss in staat om een geavanceerd computermodel voor de ontwikkeling van de symptomen van de ZvH te bouwen. Ze stelde toen een heel slimme vraag – hebben mensen van wie de ZvH snel (of langzaam) vordert, samenhangende genetische verschillen? Ze zochten naar variaties in alle genen van de TRACK-HD-deelnemers van wie de ZvH ontwikkeling ongebruikelijk was. Ze ontdekten genetische variaties buiten het ZvH-gen die leiden tot veranderingen in de snelheid van de ontwikkeling van de ZvH-symptomen. Moss merkt op dat variaties in DNA-herstelgenen de snelheid van de ZvH ontwikkeling veranderen. Dit is overweldigend bewijs dat het proces van DNA-herstelling belangrijk is bij de ZvH, hoewel de details nog niet duidelijk zijn. De duidelijke boodschap van deze studies is dat het van cruciaal belang is om cellen te helpen de CAG-herhalingen in het ZvH-gen nauwkeurig te kopiëren. Deze bevinding is alleen mogelijk dankzij duizenden ZvH familieleden die deelnemen aan studies en DNA doneren. Deze genetische studies werden gedaan met behulp van technologie die niet bestond toen de meeste deelnemers hun DNA doneerden voor onderzoek.
Chris Kay (UBC) spreekt de conferentie toe over een ander type genetische variatie – veranderingen in de volgorde van het ZvH-gen zelf. Kay brengt kleine spellingsvariaties buiten de CAG-regio van het ZvH-gen in kaart. Kay heeft een aantal variaties gevonden die veel vaker voorkomen in ZvH-genen met CAG-verlengingen dan in genen zonder die CAG-verlenging. Dit helpt ons de historische oorsprong en wereldwijde verdeling van de ZVH-veroorzakende CAG-verlenging te begrijpen. Het biedt ook zeer interessante doelen voor onderzoekers die hopen het niveau van het mutante ZVH-gen selectief te verlagen.
Christian Neri van Inserm bestudeert een eiwit genaamd FOXO en zijn rol in de ZvH. FOXO helpt hersencellen om te gaan met ‘stress’. Wetenschappers bedoelen met ‘stress’ alles wat het moeilijker maakt voor cellen om hun ding te doen. FOXO regelt veel methoden die cellen kunnen gebruiken om te overleven en om te gaan met stress.
“Deze bevinding is alleen mogelijk dankzij duizenden ZvH familieleden die deelnemen aan studies en DNA doneren.”
Matthias Mann is een pionier op het gebied van “proteomics”. Met deze technologie kunnen wetenschappers de niveaus van duizenden eiwitten in één keer nauwkeurig meten. Genen zijn opwindend, maar eiwitten doen het grootste deel van het werk van de cel. Mann’s groep heeft opmerkelijke hulpmiddelen ontwikkeld om ze te meten. De groep van Mann begint nu met de ZvH te werken en past zijn methoden toe om te proberen nieuwe manieren te vinden om de ontwikkeling van de ZvH te volgen.
Publieke vijand nummer één: mutant huntingtine
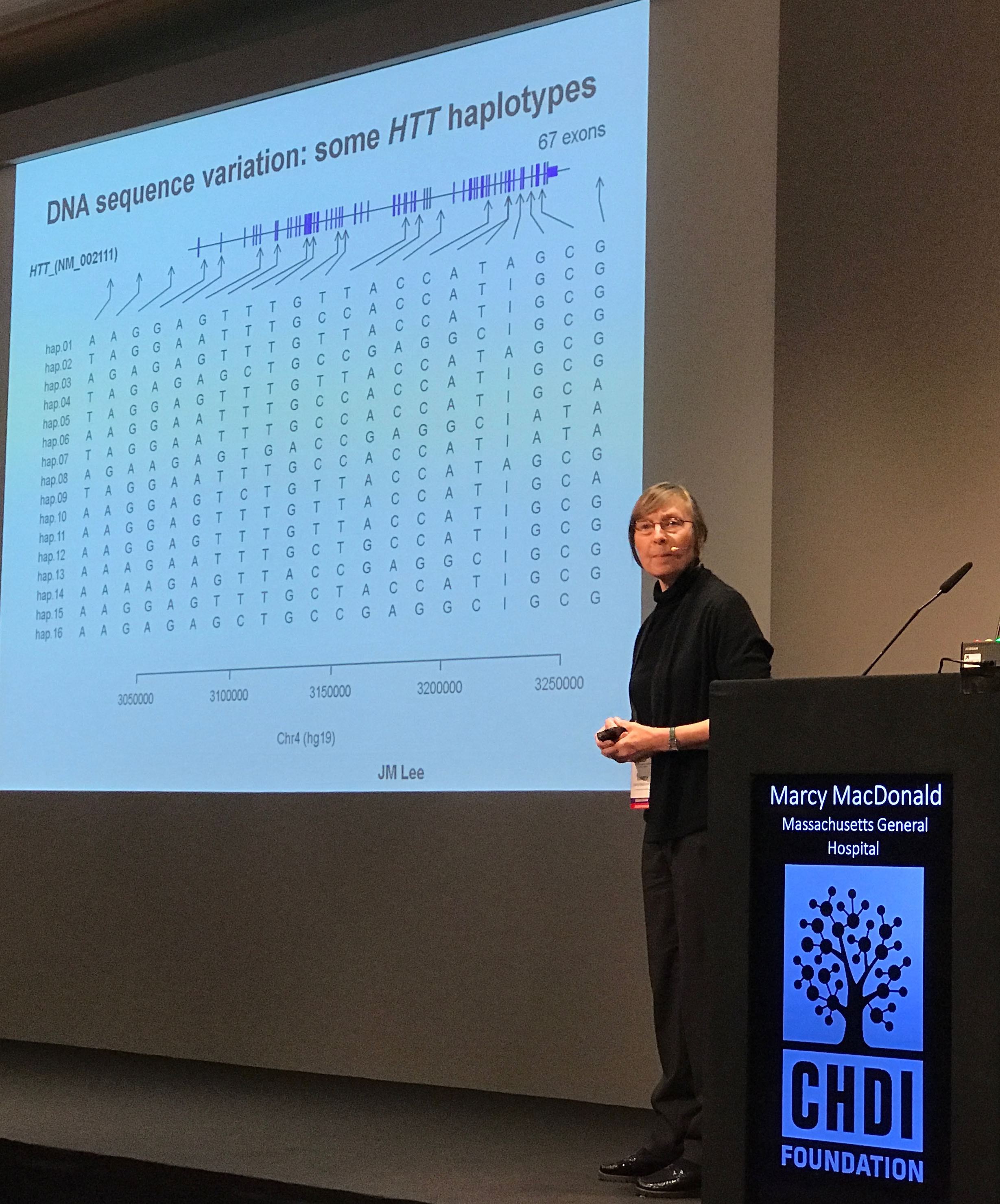
Marcy MacDonald (MGH) heeft haar carrière besteed aan het bestuderen van verschillen in het ZvH-gen. MacDonald is een belangrijk lid van het GeM-HD-consortium, die genetische variaties in kaart brengen die de ontwikkeling van de ZvH-symptomen beïnvloeden. Ze hebben met behulp van DNA van meer dan 7.000 personen een gloednieuwe variant ontdekt die de ZVH-progressie wijzigt. De nieuwe variant is zeer zeldzaam – alleen door informatie van duizenden vrijwilligers te bundelen kon het team de ontdekking doen. Darren Monckton van de Universteit van Glasgow, is geïnteresseerd in de CAG-herhaling van het ZvH-gen. We weten sinds 1993 dat verlenging van een CAG-herhaling in het ZvH-gen elk geval van de ziekte veroorzaakt. Meer recent begrijpen Monckton en andere onderzoekers dat CAG-herhalingen tijdens de levensduur van een cel nog langer kunnen worden. Het team van Monckton gebruikt nieuwe technologieën om de lengte van het ZvH CAG-kanaal bij 1.000 ZvH-patiënten nauwkeurig te meten. Ze hopen dat het vinden van zeldzame variaties in de organisatie van de CAG-herhaling ons zal helpen begrijpen hoe CAG-herhalingen langer worden. Monckton ontdekte dat DNA-herstelgenen waar Dr. Hensman Moss eerder over sprak, de spreiding van CAG-herhalingsgroottes in iemands cel beïnvloeden. (Terzijde: de CAG-telling in een genetisch testresultaat is eigenlijk de gemiddelde telling – verschillende cellen bevatten iets verschillende aantallen). Een theorie over waarom de symptomen van sommige mensen snel vorderen, is dat de CAG-herhaling in kwetsbare hersencellen kan toenemen. Genetici noemen dit ‘somatische instabiliteit’ van de CAG-herhaling. Het begrijpen van somatische instabiliteit is een belangrijke missie, want als we het zouden kunnen verminderen, kunnen we hersencellen helpen langer te overleven.
Kevin Weeks (UNC) is geïnteresseerd in RNA – de chemische tussenliggende informatie van DNA om eiwitten in cellen te maken. RNA wordt vaak gezien als een reeks letters die wordt gekopieerd uit het DNA, maar RNA vouwt zich op in complexe vormen met belangrijke rollen. Het laboratorium van Weeks bouwt precieze modellen van het RNA gemaakt van het ZvH-gen, in 3D-vorm. Het verandert naarmate het aantal CAG-herhalingen in het ZvH-gen toeneemt – meer CAG’s leiden tot grote veranderingen in de 3D-RNA-structuur. Deze vormveranderingen vormen een uniek doel voor het team van Weeks om RNA-niveaus voor het mutante gen op te sporen en misschien te verlagen. Dit opent een nieuwe manier om te voorkomen dat cellen mutant huntingtine-eiwit maken, de meest waarschijnlijke dader voor het ziek maken van cellen in de ZvH.
Hoewel de ZvH het meest voorkomt op volwassen leeftijd, richt Mark Mehler, van het Albert Einstein College of Medicine, zich op zeer vroege veranderingen. Hij vindt subtiele veranderingen in de ontwikkeling van de hersenen bij muizen met zeer lange CAG- herhalingen in het ZvH-gen. Deze veranderingen kunnen hersencellen kwetsbaarder maken op volwassen leeftijd.
Alberto Ruzo (Rockefeller) is ook geïnteresseerd in het ontwikkelingsproces – het proces waarbij een bevruchte eicel een volwassene wordt. Tijdens de ontwikkeling delen zich speciale cellen die “stamcellen” worden genoemd. Deze produceren uiteindelijk alle celtypen in een volwassen lichaam. Ruzo heeft nieuwe stamcellen gecreëerd die genetisch identiek zijn, maar dan zonder een toenemend aantal CAG-herhalingen in het ZvH-gen. Dit stelt hem in staat om het proces te bestuderen waarbij de delende stamcellen uitgroeien tot de complexe vormen die aanleiding geven tot volwassen organen. Hij observeerde veranderingen in deze vormen in cellen met langere CAG-herhalingen.
Voor meer informatie over ons openbaarmakingsbeleid, zie onze FAQ…