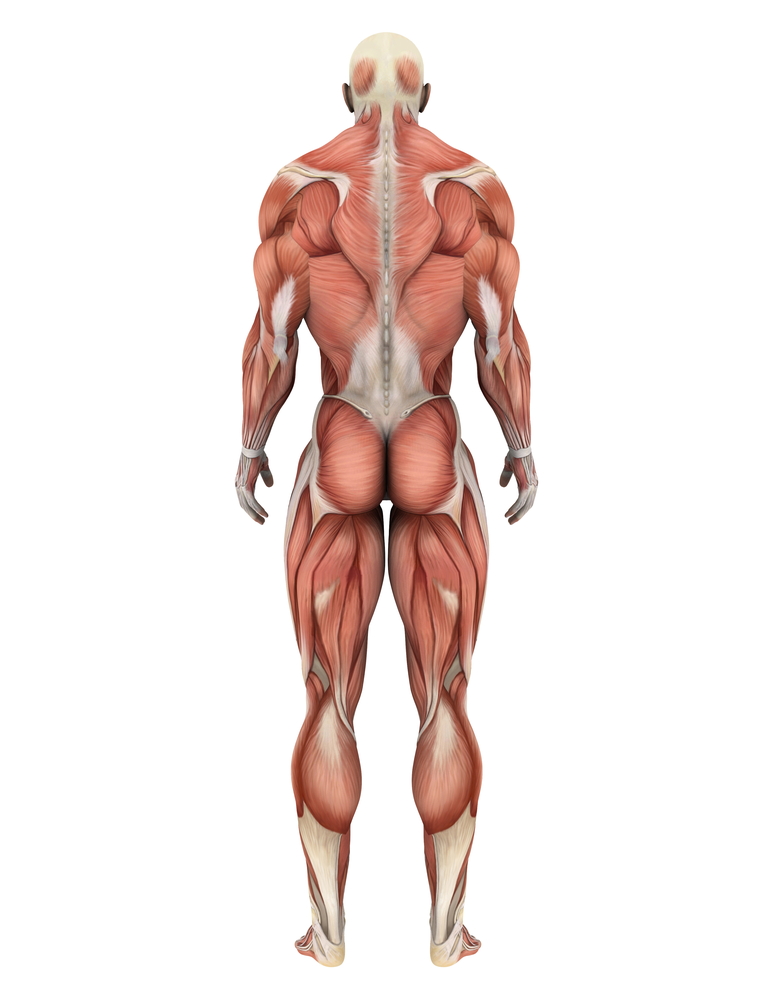
Zouden spierproblemen het inzicht in bewegingen bij de ziekte van Huntington kunnen verbeteren?
Juiste samentrekking van spieren is cruciaal voor coördinatie; procesfouten kunnen bewegingen verklaren bij de ZvH
Een juiste balans van elektrisch geladen deeltjes is nodig om spiercellen adequaat te laten reageren op prikkels. Echter, na een recente studie bij muizen met de ziekte van Huntington (ZvH) kwamen een groep wetenschappers van The California State Polytechnic University tot de conclusie dat bij de ZvH een verstoring van dit evenwicht optreedt, waardoor spiervezels zich gemakkelijker samentrekken dan zij zouden moeten doen.
Een grote beweging
Elke zorgverlener is bekend met de ‘Onheilige Drie-eenheid’ van ZvH-symptomen: chorea (ongewilde overtollige bewegingen), cognitief verlies, en gedragsverstoringen. Ondanks het feit dat de andere symptomen zich doorgaans eerder voordoen bij de patiënt, worden door artsen de ongecontroleerde bewegingen vandaag de dag nog steeds gebruikt als belangrijkste diagnostische kenmerk van de ziekte. De bewegingen zien er extreem ongecontroleerd uit: de patiënt heeft een spier die ongewild begint samen te trekken, maar de beweging die hierdoor ontstaat wordt niet afgemaakt. Dit suggereert dat de spiervezels onderling niet goed op elkaar afgestemd worden.
Helaas is de oorsprong van de ongewilde bewegingen nog mysterieuzer dan die van de andere symptomen. Hoewel elke cel in het lichaam het abnormale eiwit produceert, het eiwit dat de ziekte van Huntington veroorzaakt, lijken hersencellen het meest kwetsbaar om af te sterven gedurende het beloop van de ziekte. Daarbij is er een bepaalde groep hersencellen die afsterven, voorafgaand aan het uitgebreide verlies van hersencellen binnen de hersenen als geheel. Omdat hersencellen bij de ZvH afsterven valt de ziekte onder de categorie van ‘neurodegeneratieve aandoeningen’.
Ionen, ionen, overal ionen
Tot voor kort werd aangenomen dat alle ZvH-symptomen konden worden herleid naar problemen in de hersenen. Een team onder leiding van Dr. Andrew Voss, van de California State Polytechnic University, twijfelde aan deze aanname en besloot om de rol van spiervezels te onderzoeken.
De hersenen geven een spier opdracht om samen te trekken door een elektrisch signaal via een zenuwcel naar een spiervezel te sturen. De spiervezel is de uitvoerder van deze opdracht. Het team van Dr. Voss richtte zich op de ontvangst van dit signaal aan het einde van deze ’telefoonkabel’, niet op de oorsprong van het signaal in de hersenen.
Bepaalde cellen van het lichaam, zoals hersencellen en spiercellen, zijn ‘elektrisch actief’. Voor een goede communicatie tussen deze cellen moeten elektrische signalen omgezet worden wanneer deze spiercellen bereiken. In tegenstelling tot de meeste elektronische apparaten hebben spieren en zenuwen geen koperdraadjes, waarmee elektrische stroompjes kunnen worden verstuurd. Hoe gebeurt dit dan wel?
Zij doen dit door kleine deeltjes, atomen die een elektrische lading hebben, te transporteren naar binnen en buiten de cel. (Ieder atoom met een elektrische lading wordt een ion genoemd.) De atomen van sommige elementen, zoals natrium en chloor, hebben de neiging om gemakkelijk “op te laden”. Zo bestaat ordinair tafelzout uit niets anders dan positief geladen natrium-ionen plakkend aan negatief geladen chloor-ionen!
Voordat een boodschap vanuit de hersenen bij een spiervezel aankomt, zijn de cellen waar deze vezel uit bestaan al in een parate toestand, klaar om dat signaal te ontvangen. Positief geladen natrium wordt aangemaakt buiten de cel en wordt verhinderd om de cel binnen te komen, terwijl positief geladen kalium-ionen worden aangemaakt binnen in de cel en verhinderd om de cel te verlaten.
Wanneer de boodschap om samen te trekken arriveert, ontstaan kleine openingen in de wand van de spiercel, waar doorheen alleen positief-geladen natrium-ionen worden doorgelaten. Deze ionen komen met hoge snelheid de cel binnen., Om de verandering in de lading van de cel te compenseren, verlaten vervolgens de positief-geladen kalium-ionen de cel door “hun eigen” specifieke kanalen.
Deze gecompliceerde reeks van gebeurtenissen die uitloopt in een spiersamentrekking heet ook wel actiepotentiaal. Uiteindelijk zal de oorspronkelijke elektrische balans hersteld worden (negatief geladen chloor-ionen ondersteunen dit proces) en wordt de cel klaargemaakt om een nieuw signaal te ontvangen. Met de kennis van normale spiersamentrekkingen heeft het team van dr. Voss in een recent onderzoek bekeken of dit mechanisme bij de ZvH normaal functioneert.
“Er is niet alleen sprake van een fout in de hersenen maar ook in de spiervezels, waardoor ongewilde bewegingen bij de ZvH beter verklaard zouden kunnen worden.”
Hiertoe maakten zij gebruik van een ZvH-muismodel, waarin muizen een onderdeel van het menselijke ZvH-gen bezitten. Dit onderdeel bevat de mutatie die de ZvH veroorzaakt bij mensen. Dit model werd gekozen omdat deze goed beschreven is (het is al bijna twintig jaar bekend) en vanwege de afwijkende bewegingen en congitieve functies die binnen dit model bekend zijn. Het onderzoeksteam heeft alle experimenten uitgevoerd gebruik makend van spiervezels die afkomstig waren van de ZvH-muizen. Deze spiervezels werden blootgesteld aan diverse elektrische prikkels (schokken). Het is overbodig om aan te tekenen, dat menselijke vrijwilligers nogal moeilijk hiervoor te vinden zijn.
De schokkende resultaten
De verkregen metingen waren allen afkomstig van spiervezels die gekoppeld waren aan een aantal kleine elektrodes en op deze manier verscheidene elektrische stroompjes kregen aangeboden. Allereerst werd een signaal, afkomstig uit de hersenen, nagemaakt aan de hand van een serie elektrische stroomstoten.
Zowel spiervezels van ZvH-muizen en ‘gewone’ muizen reageerden op normale wijze op de aangeboden stroomstoten. De spiervezels van de ZvH-muizen deden er echter veel langer over om na de stroomstoot hun elektrische lading weer naar normaal te herstellen. Dit is de fase van het actiepotentiaal waarin kalium-ionen zich uit de cel verplaatsen.
Tevens bleek de sterkte van de stroomstoot die nodig was om een actiepotentiaal tot stand te brengen veel lager binnen ZvH-spiervezels. Dit suggereert dat deze spiervezels gemakkelijker neigen samen te trekken. Daar komt nog bij dat verschillende ZvH-vezels na een stroomstoot die niet sterk genoeg zou moeten zijn om een actiepotentiaal te veroorzaken, ook samentrokken.
Spiervezels van ZvH-muizen zijn klaarblijkelijk veel gevoeliger voor deze stimuli (“overprikkelbaar”). De auteurs speculeerden dat deze overprikkelbaarheid verklaard zou kunnen worden door afname in stroom van kalium- en/of chloor-ionen in deze cellen.
Een volgende serie stroomstoten bracht aan het licht dat de kanalen in vezels van ZvH-muizen minder en moeizamer elektrische lading doorlieten gedurende een bepaalde tijd. dan kanalen van gewone vezels. De auteurs concludeerden dat deze beperkingen eenvoudigweg verklaard worden door een afname in aantal functionele kalium- en chloor-kanalen zijn. Om deze reden onderzochten zij de processen die resulteren in de aanmaak van deze kanalen.
De code voor de structuur van een eiwit (zoals een ion-kanaal) bevindt zich in het DNA van een organisme. Na aflezen van deze code wordt eerst een tijdelijke tussenstof gemaakt, genaamd RNA. Uit het RNA wordt vervolgens een specifiek eiwit gevormd.
Bij het bestuderen van de spiervezels van de ZvH ontdekten de wetenschappers een afname van RNA, waaruit chloor- en kaliumionkanalen wordt gemaakt.

Dus zij hadden de juiste conclusie getrokken: de afwijkingen in elektrische activiteit, die zij zagen bij ZvH-spiervezels waren het gevolg van een tekort aan specifieke ionkanalen binnen spiercellen, die noodzakelijk zijn voor een normale functie van deze cellen.
Wat betekent dit voor de ZvH?
Na door deze gecompliceerde elektrofysiologie en moleculaire genetica te hebben geworsteld, rijst de vraag: wat is de betekenis van deze studie nu eigenlijk voor de gemeenschap van mensen met de ziekte van Huntington. Ten eerste heeft deze studie een zeer interessante observatie opgeleverd: er is niet alleen sprake van een defect in de hersenen, maar ook in spiervezels van mensen met de ZvH. Hiermee is het inzicht verbetert in het mechanisme, die ten grondslag ligt aan de ongecontroleerde bewegingen bij de ZvH.
Bij deze interessante bevindingen moeten een aantal kanttekeningen worden geplaatst. Ten eerste is deze studie uitgevoerd op een muismodel van de ziekte. Ondanks dat dit een algemeen geaccepteerd model is, levert dit nog geen garantie, dat dezelfde resultaten ook gevonden worden bij mensen met de ZvH, daar waar het uiteindelijk om draait.
Belangrijker nog, we staan nog steeds ver af van iets, dat nuttig zou kunnen zijn om de ziekte mee te behandelen. Zelfs als dezelfde verschijnselen aan de orde zouden zijn bij mensen met de ziekte, zullen we nog steeds een manier moeten vinden om deze problemen te verhelpen.
Ten slotte, zelfs als de bevindingen van deze studie ook gevonden worden bij mensen en er een effectieve behandeling kan worden bedacht (spiervezels zijn in ieder geval makkelijker bereikbaar dan hersencellen), dan betekent dit, dat alleen dat de overtollige bewegingen verholpen zouden kunnen worden. Het zou geen effect hebben op de andere symptomen van de ziekte, zoals afwijkingen in persoonlijkheid en cognitie. Uiteraard weet elke hulpverlener dat alleen al verbetering op het gebied van ongewilde bewegingen enorm nuttig en behulpzaam is, dat lichamelijk beperkingen zouden verbeteren en ondersteuning van mensen met de ZvH gemakkelijker zou gaan.
Het belangrijkste is dat momenteel alle medicatie gericht op het verhelpen van motorische symptomen bij de ZvH aangrijpt in de hersenen. Dit artikel laat zien dat spieren ook een potentieel doelwit zijn en dit onderzoek schept nieuwe aanknopingspunten voor aanvullende studies. Medicijnen, die binnen de hersenen aangrijpen om ongewilde bewegingen te verbeteren, hebben als belangrijk nadeel dat de kans op bijwerkingen groot is. Behandelingen die in lijn met de bevindingen van deze studie direct aangrijpen op het niveau van spieren zouden hierin een vooruitgang zijn.
Leer meer
- Link naar het originele verslag in the Proceedings of the National Academy of Sciences of the USA (full article requires payment or subscription)
- In de war geraakt? Hier is een link naar een hele fraaie animatie die beschrijft hoe deze actie potentialen werken.
- Link naar het Voss laboratorium, de thuisbasis van het hierboven beschreven onderzoek.
For more information about our disclosure policy see our FAQ…


