
ASO-genonderdrukking reikt verder en houdt langer aan
Het onderdrukken van het Huntington-gen met ASO-medicijnen reikt verder, houdt langer aan en is veilig. Binnenkort een menselijke proef?
Medicijnen genaamd antisense-oligonucleotiden, of ASO’s, zijn een manier om het gen dat de ziekte van Huntington veroorzaakt te onderdrukken. Een nieuwe publicatie in het tijdschrift Neuron suggereert dat ASO-genonderdrukking verder reikt in de hersenen dan andere methoden, langer aanhoudt en veilig is.
We hebben gretig gewacht op ontwikkelingen op het gebied van genonderdrukking, en daarom waren we super enthousiast om een belangrijk nieuw onderzoek te lezen dat vandaag is gepubliceerd in het toptijdschrift Neuron. Een groep onderzoekers, onder leiding van Dr. Don Cleveland aan de Universiteit van Californië San Diego, in samenwerking met de farmaceutische bedrijven Isis pharmaceuticals, Genzyme en Novartis, hebben antisense-oligonucleotiden (ASO’s) ontwikkeld voor de ziekte van Huntington. Dus waar zijn ze mee bezig geweest en wat hebben ze ontdekt?
Genetica herhaling

Afbeelding: www.biocomicals.com door Alper Uzun, PhD
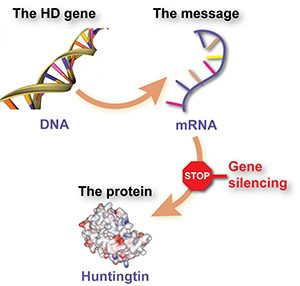
Het Huntington-gen is slechts een van de ongeveer 25.000 genparen, gemaakt van DNA, die de code dragen voor het maken van eiwitten; de bouwstenen voor de cellen waaruit ons lichaam bestaat. Er zijn een paar stappen tussen de DNA-‘code’ en het uiteindelijke eiwit. Een van die stappen betreft messenger RNA, of mRNA.
Het HD-gen is de code die, wanneer vertaald, HD-mRNA maakt. Het is het mRNA dat een cel vertelt hoe het huntingtine-eiwit te maken. Mensen met de ziekte van Huntington hebben één normale kopie en één uitgebreide kopie van het gen, dus ze maken ook twee verschillende soorten mRNA.
Sinds het HD-gen bijna 20 jaar geleden werd geïdentificeerd, proberen wetenschappers te begrijpen wat het doet, hoe het de symptomen van HD veroorzaakt en hoe het effectief kan worden uitgeschakeld.
Het gen uitschakelen
Er zijn een aantal mogelijke methoden om het HD-gen uit te schakelen. De misschien wel meest bekende is RNA-interferentie, ook bekend als RNAi of soms siRNA.
Een andere benadering gebruikt een iets ander molecuul genaamd antisense-oligonucleotiden, of ASO’s.
ASO’s zijn een soort kruising tussen DNA en mRNA. Ze zijn chemisch vergelijkbaar met DNA, maar bestaan uit een enkele streng zoals mRNA. Net als andere genonderdrukkende medicijnen zijn ze ontworpen om aan het HD-mRNA te plakken en de cel te vertellen het te vernietigen, waardoor wordt voorkomen dat het abnormale huntingtine-eiwit ooit wordt gemaakt.
De theorie hierachter is dat als je voorkomt dat het abnormale huntingtine-eiwit wordt gemaakt, je de schadelijke effecten ervan op cellen voorkomt, en daardoor symptomen vermindert of vertraagt.
In de afgelopen paar maanden hebben we goed nieuws gehoord van verschillende groepen die werken aan RNAi-medicijnen, maar tot voor kort hadden de ASO-onderzoekers niet zoveel gepubliceerd. Dat is net veranderd met deze laatste publicatie, die ons op de hoogte brengt van enkele jaren hard werk.
Klinische studies bij mensen met ASO’s voor andere neurologische aandoeningen zijn al begonnen, maar de situatie bij HD is vertraagd door enkele onbeantwoorde vragen.
Het effect van ASO’s
In dit gloednieuwe werk heeft een slimme groep onderzoekers gekeken naar de effecten van het gebruik van ASO’s in 3 verschillende muismodellen van HD, en ook in een apenmodel (het op een na beste na mensen in termen van diermodellen), om te proberen de antwoorden op een aantal verschillende vragen te vinden.
“ASO’s behandelen delen van de hersenen die andere genonderdrukkingstechnieken niet konden bereiken”
Bij de apen werd het medicijn in het ruggenmergvocht geïnjecteerd – een veel minder invasieve procedure dan het in de hersenen te injecteren, en een die de voorkeur zou hebben voor menselijke patiënten.
1. Wat gebeurt er als je een ASO toedient, en hoe lang houdt het aan?
Wel, ze infuseerden de ASO’s in de hersenkamers (met vloeistof gevulde ruimtes in de hersenen) gedurende twee tot drie weken. Dit leidde tot verminderde niveaus van het abnormale huntingtine-eiwit in veel gebieden die bekend staan als belangrijk in de hersenen, waaronder het striatum, dat het meest prominent wordt aangetast bij de ziekte van Huntington. ASO’s konden zich veel verder in de hersenen verspreiden dan we hebben gezien met RNAi-medicijnen.
Bovendien bleven de niveaus lange tijd laag – tot drie maanden na het stoppen van de infusie.
2. Wat gebeurde er met de symptomen?
Onderzoekers kunnen de symptomen van diermodellen monitoren met behulp van tests die bewegingen en gedrag meten. De dieren die met ASO’s werden behandeld, verbeterden in vergelijking met hun onbehandelde tegenhangers. Nog beter, de verbetering hield lang aan – en niet alleen terwijl de eiwitniveaus laag bleven. Symptomen waren nog steeds beter enkele maanden nadat de niveaus van abnormaal huntingtine-eiwit waren teruggekeerd naar de niveaus van voor de behandeling.
Dit ondersteunt het idee dat de hersenen mogelijk slechts een beetje hulp nodig hebben om de effecten van het HD-gen te overleven. Een prominente HD-onderzoeker, Carl Johnson, bedacht de term ‘huntingtine-vakantie’ om te suggereren dat een korte pauze van het schadelijke eiwit alles kan zijn wat nodig is om de balans in het voordeel van herstel te laten doorslaan.
3. Wanneer is het beste moment om behandeling te geven?
Deze studie suggereert dat vroege behandeling waarschijnlijk beter is.
Motorische symptomen in een bepaald muismodel verbeterden binnen een maand na behandeling, en bleven verbeteren totdat de HD-muizen er niet anders uitzagen dan normale muizen. Gedragssymptomen waren binnen 2 maanden na behandeling weer normaal.
Toen oudere muizen met meer symptomen werden behandeld, verbeterden hun motorische en gedragssymptomen wel, maar het duurde veel langer voordat verbeteringen merkbaar waren, en ze herstelden niet zoveel als de jongere, gezondere muizen.
4. Wat gebeurt er als je het ‘normale’ HD-mRNA blokkeert?
Dit is een van de belangrijkste vragen die ons tegenhoudt om trials bij de ziekte van Huntington te starten. We weten dat het huntingtine-eiwit essentieel is voor vroege ontwikkeling, aangezien muisembryos die zo zijn gemanipuleerd dat ze geen huntingtine produceren, sterven voordat ze geboren worden. Is het veilig om de productie van zowel het normale als het abnormale huntingtine-eiwit bij volwassenen uit te schakelen?
Dankzij dit werk, en het werk van andere genonderdrukkingsonderzoekers, komen we dichter bij een antwoord. Het uitschakelen van normaal HD-mRNA gedurende maximaal 3 maanden bij gezonde apen werd goed verdragen. In de diermodellen van HD veranderde het uitschakelen van zowel het normale als het abnormale mRNA niets aan de mate van herstel en had het geen slechte effecten.
Het enige mogelijke struikelblok nu is dat mensen gevoeliger kunnen zijn voor het hebben van minder huntingtine dan elk dier waarin we de medicijnen zouden kunnen testen. Alleen een proef met patiënten zal ons dat met zekerheid vertellen.
Dit is allemaal goed nieuws
We hebben nu bewijs dat ASO’s delen van de hersenen behandelen die andere genonderdrukkingstechnieken niet konden bereiken. Niet alleen dat, maar een kortdurende infusie met ASO’s was voldoende om de progressie van symptomen in diermodellen van de ziekte van Huntington te vertragen. En de omkering van symptomen houdt veel langer aan dan verwacht, zelfs nadat de niveaus van het abnormale huntingtine-eiwit weer normaal zijn geworden.
Wat gebeurt er nu?
We weten dat mensen die het uitgebreide HD-gen dragen vele jaren volkomen gezond kunnen blijven, ondanks dat ze het abnormale huntingtine-eiwit vanaf de geboorte produceren.
Misschien is een eenmalige behandeling met ASO’s, of een behandeling eens per jaar, voldoende om ‘de ziekteklok te resetten’ door de productie van het huntingtine-eiwit lang genoeg te blokkeren om cellen de ophoping te laten opruimen. De volgende fase in het onderzoek van deze groep zal zijn om te kijken hoe lang een enkele ASO-injectie zal aanhouden.
Dit werk suggereert ook dat infusie in het ruggenmergvocht goed genoeg zou kunnen zijn voor ASO-medicijnen. Dat is geen wandeling in het park, maar is relatief eenvoudig vergeleken met het aanbrengen van buisjes en pompen om medicijnen rechtstreeks in de hersenen te krijgen.
We moeten ook uitzoeken hoeveel ASO nodig zal zijn om een effect bij mensen te produceren, wanneer en hoe lang het moet worden gegeven, en voorbereid zijn op onverwachte bijwerkingen.
Maar het lijkt erop dat we steeds dichter bij menselijke HD-genonderdrukkingsproeven komen. En met verschillende groepen die allemaal op de rand van proeven staan, en gretig zijn om de eerste te zijn die hun medicijn bij patiënten testen, is het echt een spannende tijd voor genonderdrukking bij HD.
Meer informatie
Bronnen & Referenties
Voor meer informatie over ons openbaarmakingsbeleid, zie onze FAQ…


