
Baby’s krijgen: een gezin stichten, op de ZvH-manier
Baby’s krijgen: HDBuzz’s hoofdartikel – bijgewerkt voor 2024 – over vruchtbaarheidstechnologieën die risicodragers kunnen helpen om ZvH-vrije kinderen te krijgen
Voor mensen met risico op de ziekte van Huntington kan het krijgen van een baby die ZvH zou kunnen erven de beslissingen rond gezinsplanning extreem moeilijk maken. Dit artikel legt de beschikbare opties uit en hoe moderne voortplantingswetenschap nu al verschil kan maken voor families die door ZvH worden geraakt.
Inhoudswaarschuwing Dit artikel beschrijft kwesties rond vruchtbaarheid, moeilijke keuzes en medische procedures, waaronder zwangerschapsafbreking.
Niet alle hier beschreven technieken zijn overal beschikbaar, en in sommige landen kunnen ze grote kosten met zich meebrengen. Dus als je over een van deze opties nadenkt, raden we je aan contact op te nemen met een gespecialiseerde genetisch counselor voor persoonlijk advies. Hoe eerder je dit doet, hoe meer opties je hebt.

Inleiding
Veel mensen met de ziekte van Huntington, of met risico erop, willen graag weten of er manieren zijn om kinderen te krijgen zonder de ziekte door te geven aan de volgende generatie. Het korte antwoord is ja!
Dankzij genetische wetenschap en voortplantingstechnologieën zijn er verschillende keuzes beschikbaar voor mensen met risico op de ziekte van Huntington, om ervoor te zorgen dat toekomstige kinderen geen risico lopen op het ontwikkelen van ZvH. Dit geldt voor mensen die getest zijn en een ZvH-genexpansie dragen, maar er kunnen ook opties zijn voor mensen die zelf kiezen om geen ZvH-genetische test te ondergaan.
Allereerst: er hoeft niets te veranderen
Hoewel dit artikel zich vooral richt op de opties voor het krijgen van ZvH-vrije kinderen, is het belangrijk om te weten dat het krijgen van een kind zonder genetische testen zeker een optie is voor ouders met risico op de aandoening.
Zoals elk HDBuzz-artikel bevestigt, maken wetenschappers echte vooruitgang in het vinden van behandelingen voor de ziekte van Huntington. Hoewel we niets kunnen garanderen of een vaste tijdlijn kunnen beloven, geloven we sterk dat er een tijd zal komen waarin risicokinderen geboren worden in een wereld waar ZvH een behandelbare aandoening is.
Bovendien is er altijd een kans dat het kind de ZvH-genexpansie niet erft en daarom nooit ZvH zal ontwikkelen.
Sommige mensen willen misschien ZvH-vrije kinderen garanderen, maar opties zijn mogelijk niet voor hen beschikbaar, bijvoorbeeld vanwege locatie, financiële ondersteuning of religieuze overtuigingen.
Het krijgen van een kind met risico op ZvH kan een punt van discussie en debat zijn binnen de ZvH-gemeenschap. Hoewel mensen het misschien niet eens zijn met de beslissingen die anderen nemen, is het belangrijk om te onthouden dat iedereen het recht heeft om gerespecteerd te worden bij het maken van hun eigen beslissingen.
De Huntington Disease Youth Organisation heeft enkele hulpmiddelen beschikbaar om ZvH en genetisch risico op een leeftijdsgeschikte manier met kinderen te bespreken:
Sommige mensen vinden dat ze geen risico willen nemen en willen het risico op het doorgeven van ZvH volledig vermijden. Daar komen genetische testtechnieken van pas. Deze opties zijn beschikbaar ongeacht of jij of je partner risico loopt op ZvH.
Wat zijn mijn genetische testopties?
Dankzij genetisch testen kunnen we het risico op ZvH identificeren bij een foetus tijdens een zwangerschap, of bij embryo’s in het lab.
Het testen van een foetus tijdens de zwangerschap wordt prenatale testing genoemd. Het testen van embryo’s in het lab is een vorm van in-vitrofertilisatie of IVF, en wordt pre-implantatie genetische test of PGT genoemd.
Als jij of je partner genetisch getest zijn en bevestigd is dat je een ZvH-genexpansie draagt, kun je directe testen laten doen tijdens de zwangerschap of via PGT, om te bevestigen of de zwangerschap of het embryo de ZvH-genexpansie heeft geërfd.
Sommige mensen willen ZvH-vrije kinderen zonder zelf de gentest te ondergaan. Daar zijn ook opties voor! Deze opties maken gebruik van ingewikkeldere versies van dezelfde methoden. Dus eerst bespreken we hoe het werkt voor stellen waarvan één partner al een positieve ZvH-gentest heeft gehad.
Pre-implantatie Genetische Test (PGT)
Pre-implantatie genetische test is een manier om een ZvH-vrij kind te krijgen zonder een zwangerschapsafbreking te hoeven overwegen. Het kan echter een lang, uitdagend en duur proces zijn.
PGT houdt in dat eicellen en zaadcellen worden gebruikt om embryo’s in een lab te creëren, vervolgens de ZvH-test op de embryo’s uit te voeren, en alleen de ZvH-negatieve embryo’s in de baarmoeder te plaatsen.
Het PGT-proces
PGT is IVF met een extra stap van genetisch testen. IVF is een medische procedure waarbij hormoonmedicatie wordt gebruikt om de eiceldonor meer eicellen dan normaal te laten produceren. Hormoonmedicatie kan injecties inhouden om de medicijnen in het lichaam toe te dienen.
De eicellen worden dan verzameld en bevrucht met een zaadmonster.
De bevruchte eicellen ontwikkelen zich tot embryo’s, die in het laboratorium tot vijf dagen worden gekweekt tot ze een klein celklompje zijn. In dit stadium worden een of twee cellen uit elk embryo verwijderd en opgestuurd voor genetisch onderzoek terwijl de embryo’s worden ingevroren en bewaard. Het verwijderen van cellen in dit vroege ontwikkelingsstadium heeft geen invloed op hoe het embryo zich ontwikkelt.
Embryo’s waarvan is vastgesteld dat ze geen risico lopen op het ontwikkelen van ZvH worden verder bewaard. Afhankelijk van het land waar je bent, worden een of twee van deze risicovrije embryo’s dan in de baarmoeder geplaatst.
Ongeveer twee weken nadat de embryo’s zijn geplaatst, wordt een zwangerschapstest uitgevoerd op een bloedmonster. Als de plaatsing succesvol is geweest, verloopt de zwangerschap verder normaal.
De nadelen van PGT
Het proces van het stimuleren van het vrijkomen van eicellen, het verzamelen van eicellen, het bevruchten buiten het lichaam en het terugplaatsen van embryo’s is altijd een tijdrovend en uitputtend proces. Het kan ook gevaarlijk zijn, met risico’s dat de persoon ziek wordt.
Er kunnen verschillende dingen misgaan, zoals dat er niet genoeg eicellen of embryo’s worden geproduceerd. Er is ook meer kans op een tweeling met PGT, wat zwaarder en riskanter is.
Bovenop de risico’s van de procedure kan er ook iets misgaan met het genetische deel van PGT. Embryo’s kunnen beschadigd raken wanneer cellen worden verwijderd, en soms werkt de ZvH-test niet omdat er niet genoeg DNA is. Door pech kunnen alle embryo’s de ZvH-mutatie hebben.
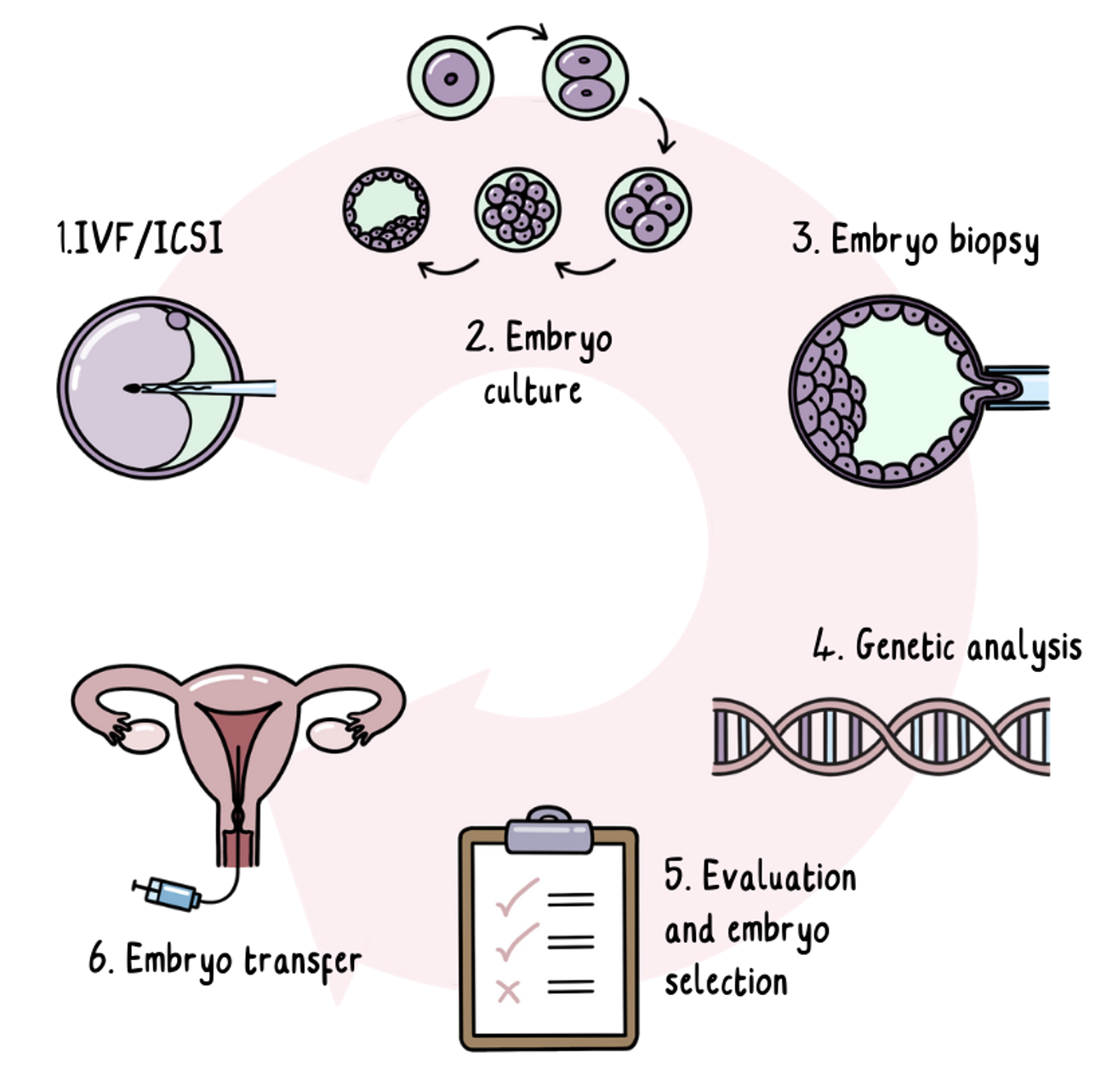
Afbeeldingscredit: @gcnotes
Uiteindelijk is soms maar één embryo beschikbaar voor implantatie – en soms helemaal geen. Bovendien kan een zwangerschap mislukken na implantatie. Over het algemeen geeft elke PGT-poging 20-30% kans op een ZvH-vrije zwangerschap. Dit slagingspercentage verschilt per PGT-centrum en is afhankelijk van verschillende factoren.
Vrouwen onder de 35 hebben de hoogste slagingspercentages – nog een reden om vooruit te denken over vruchtbaarheid. Helaas zijn de slagingskansen boven de 40 klein.
Hoeveel kost PGT?
PGT is duur. De kosten liggen rond de US $20.000 (£15.000 of €18.000) per poging.
Zorgverzekeringen dekken meestal niet de kosten van PGT/PGD. In sommige landen financiert het openbare zorgsysteem enkele PGT-pogingen – bijvoorbeeld drie pogingen in het VK – maar zelfs dit kan variëren binnen individuele landen, en kan beperkt zijn tot stellen zonder bestaande kinderen.
Extra embryo’s die geen risico lopen op ZvH kunnen worden bewaard. Dit brengt echter ook kosten met zich mee die variëren afhankelijk van de bewaartijd.
Als dit een optie is die je overweegt, raden we aan contact op te nemen met je lokale genetische dienst voor een gesprek over geschiktheid, verwijzing en bijbehorende kosten.
Testen tijdens de zwangerschap
Het is mogelijk om een genetische test uit te voeren tijdens de zwangerschap om te zien of de zich ontwikkelende baby (foetus) de genexpansie draagt die ZvH veroorzaakt. Dit wordt prenatale testing genoemd.
Beslissen of je een foetus wilt laten testen is een moeilijke beslissing. Het is belangrijk om te begrijpen dat prenatale testing bij ZvH alleen wordt uitgevoerd met het begrip dat als het resultaat zou aantonen dat de foetus de ZvH-genexpansie draagt, de zwangerschap zal worden afgebroken. Dit is een immens uitdagende en persoonlijke keuze.
Het is belangrijk om zorgvuldig na te denken over prenatale testing voor ZvH, en hoe je je voelt over zwangerschapsafbreking, voordat je zwanger wordt.
Eenmaal zwanger is er zeer weinig tijd om de informatie over de prenatale test te verwerken en deze belangrijke beslissingen te nemen, aangezien de tests vroeg tijdens een zwangerschap moeten worden uitgevoerd.
Het testen van een zwangerschap, maar niet doorgaan met een afbreking na een positief testresultaat, zou het recht van het kind wegnemen om later in het leven zelf te kiezen of het de genetische test wil ondergaan. De meeste mensen met risico op ZvH kiezen er immers voor om de test niet te doen voordat ze symptomen ontwikkelen. We weten dat er grote problemen kunnen ontstaan wanneer een kind vanaf de geboorte wordt geïdentificeerd als iemand die ZvH zal ontwikkelen.
Bovendien kan de meeste testing tijdens de zwangerschap alleen worden gedaan als er vooraf tests zijn uitgevoerd bij het stel of andere familieleden. Vaak is er niet genoeg tijd om dit voorbereidende werk te doen wanneer een zwangerschap al is begonnen.
Invasieve prenatale testing
Meestal en het meest betrouwbaar wordt een procedure genaamd chorionvillusbiopsie of CVS uitgevoerd tijdens de vroege zwangerschap om de foetus te testen. CVS houdt in dat er een klein monster van de placenta wordt afgenomen dat het DNA in de foetus vertegenwoordigt.
CVS is een snelle procedure in de polikliniek, en in sommige landen wordt het onder plaatselijke verdoving gedaan. Afhankelijk van waar de placenta aan de baarmoederwand is gehecht, wordt een zeer dunne naald door de baarmoederhals of door de huid van de buik gestoken, waarbij een echoscanner wordt gebruikt om deze te geleiden. Er wordt dan een klein celmonster uit de placenta genomen.
Deze cellen kunnen worden gebruikt om te testen op de ZvH-genexpansie. Sommige genetische centra bieden ook testing aan voor drie veel voorkomende chromosoomsyndromen als onderdeel van de CVS-genetische test.
CVS wordt meestal uitgevoerd tussen 11 en 12 weken zwangerschap maar niet later dan 15 weken. Een vroege daterende echo is vaak vereist voordat een CVS plaatsvindt.
De belangrijkste complicatie van deze procedure is een klein risico op miskraam. Elk centrum zal specifieke informatie hebben over het risico op miskraam na een CVS. Neem contact op met je lokale centrum als je meer wilt weten.
Een vruchtwaterpunctie is een andere invasieve prenatale testtechniek, vergelijkbaar met CVS, maar neemt een monster van vruchtwater in plaats van placenta. Dit kan worden uitgevoerd vanaf 16 weken. Dit geeft daarom een resultaat op een veel later tijdstip in de zwangerschap en kan beslissingen rond zwangerschapsafbreking nog uitdagender maken.
Als de genetische test positief is, kan een afbreking meestal onder algehele verdoving worden uitgevoerd tot ongeveer 12-13 weken, afhankelijk van de wetgeving van het land. Helaas kan er soms een wachtlijst zijn voor deze procedure.
In sommige landen kan zwangerschapsafbreking later worden uitgevoerd door de bevalling in te leiden; de beschikbaarheid van deze optie is echter weer afhankelijk van de wetgeving van het land.
Wat als ik zelf geen gentest wil ondergaan?
Er zijn manieren om ZvH-vrije kinderen te krijgen zonder dat de risicodragende partner zelf getest hoeft te worden.
Ze gebruiken dezelfde basismethoden die we hebben beschreven – prenatale testing of PGT – met een genetische twist om ‘hoog risico’ zwangerschappen of embryo’s te identificeren zonder de ZvH-genstatus van de risicodragende partner te onthullen.
De twist is een paar methoden die exclusietesting of non-disclosure testing worden genoemd. Deze vereisen meer voorbereiding en planning, en er zijn situaties waarin het niet mogelijk is, dus als dit de juiste optie voor jou lijkt: vraag vroeg deskundig advies.
Hoe werkt exclusietesting?
Exclusietesting vereist ten minste drie bloedmonsters. Een van elk van het stel dat hun gezin wil uitbreiden en idealiter een van zowel de moeder als vader van de persoon met risico op het ontwikkelen van ZvH. Deze techniek is soms niet mogelijk zonder een bloedmonster van de ouder die ZvH heeft.
We weten dat ieder van ons één kopie van het ZvH-gen van elke ouder zal erven. De aangedane grootouder zal één normale kopie van het ZvH-gen hebben en één geëxpandeerde kopie van het ZvH-gen. We kunnen deze genen ‘AA’ noemen. We weten niet welke is doorgegeven aan hun volwassen kind – en die persoon wil niet getest worden om erachter te komen.
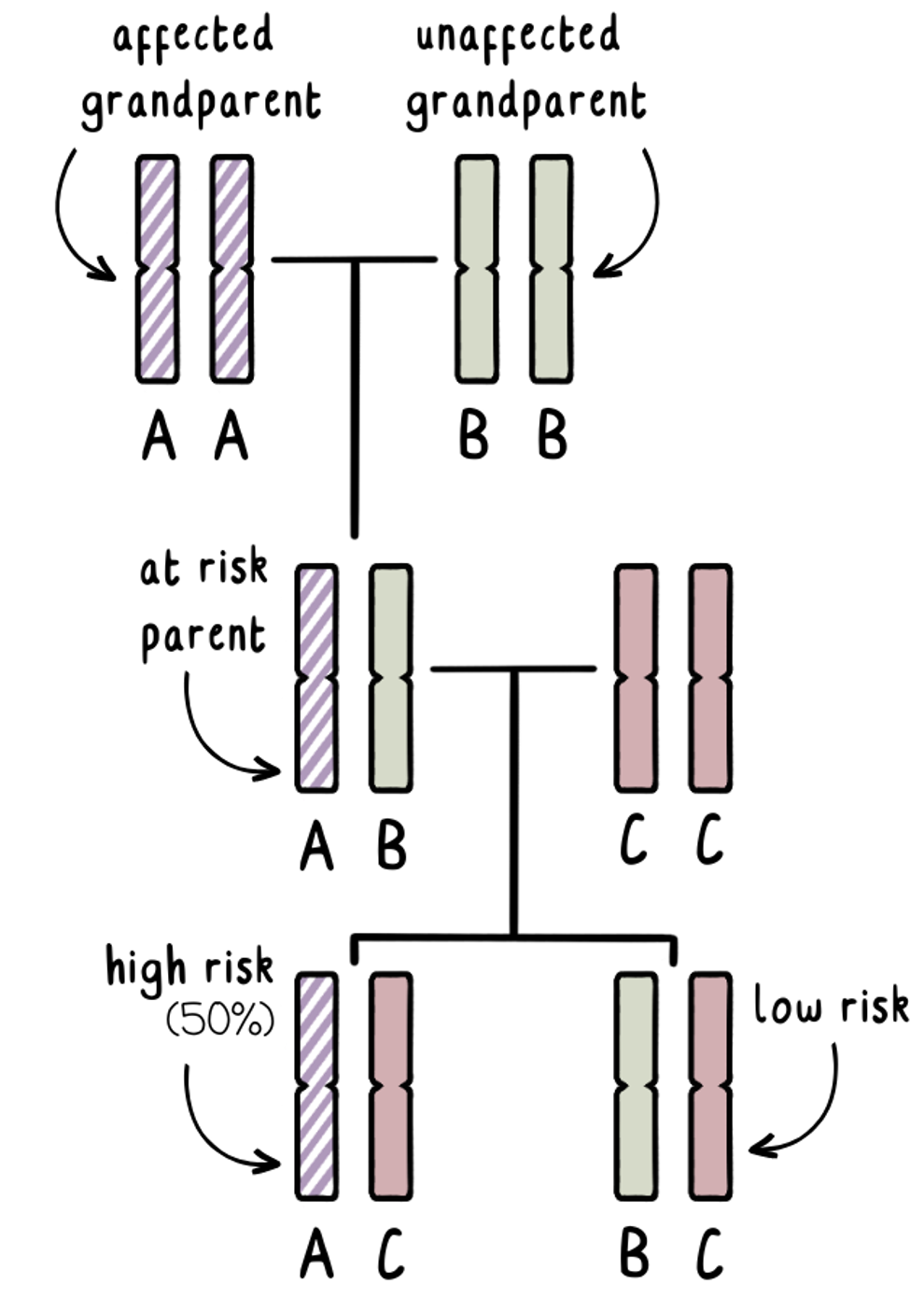
Afbeeldingscredit: @gcnotes
De niet-aangedane grootouder zal twee normale kopieën van het ZvH-gen hebben. We kunnen deze ‘BB’ noemen.
De volwassene met risico zal een combinatie van A en B hebben, waarbij het A-gen 50% kans heeft om de mutatie te dragen.
Als zij een gezin willen stichten zonder genetische testing om hun eigen risico te bepalen, kunnen we exclusietesting gebruiken tijdens een prenatale test of PGT om te identificeren of de foetus of het embryo een A-gen van de aangedane grootouder heeft geërfd, of een B-gen van de niet-aangedane grootouder. Dit vertelt ons of de zwangerschap hoog risico of laag risico zou zijn.
Cruciaal is dat exclusietesting de grootouder van oorsprong identificeert, zonder ons te vertellen of het geëxpandeerde ZvH-gen is geërfd. Als we daar achter zouden komen, zou het ons de resultaten van de risicodragende ouder kunnen vertellen – wat we juist proberen te vermijden!
De keerzijde hiervan is dat sommige hoog-risico embryo’s geen ZvH-mutatie dragen, wat zou betekenen dat mogelijk een zwangerschap wordt afgebroken of embryo’s worden weggegooid die misschien helemaal geen risico op ZvH hadden.
Non-disclosure PGT
Non-disclosure is een variant op PGT die risicodragers in staat stelt om ZvH-vrije kinderen te krijgen zonder hun eigen genetische status te ontdekken. Deze optie is niet in elk land beschikbaar, dus het is belangrijk om contact op te nemen met je lokale genetische dienst om te weten of dit een optie is die in jouw regio beschikbaar is.
Als een risicopaar kiest voor non-disclosure PGT, zou het bloedmonster van de risicodragende persoon worden getest op de ZvH-mutatie. De risicodragende persoon zou niet op de hoogte worden gesteld van het resultaat van deze test, en ook geen van de zorgverleners die de risicodragende persoon ontmoet – alleen de professionals in het vruchtbaarheidslaboratorium zouden het resultaat kennen.
De PGT begint dan, met eicelafname en het genereren van embryo’s. Als het ‘geheime’ testresultaat van de risicodragende persoon aantoonde dat zij een ZvH-genexpansie hadden, worden de embryo’s getest op ZvH, en worden alleen die zonder de ZvH-genexpansie teruggeplaatst voor een mogelijke zwangerschap.
Het stel wordt niet verteld hoeveel eicellen er worden geoogst, hoeveel er succesvol worden bevrucht, of hoeveel embryo’s er worden geïmplanteerd. Als er geen embryo’s zijn zonder een HD-genexpansie, stopt de cyclus daar en wordt het stel verteld dat de bevruchting is mislukt, maar niet waarom.
IVF kan om vele redenen mislukken, dus het niet zwanger worden kan niet worden geïnterpreteerd als een teken dat de persoon met risico het HD-gen heeft.
Andere opties
Een manier om HD-vrije kinderen te krijgen is door donor-eicellen of -sperma te gebruiken in plaats van die van de persoon met risico. Beslissen om een kind te krijgen met hulp van een donor is een moeilijke beslissing, maar vermijdt de noodzaak om beëindiging van een zwangerschap te overwegen. Het kan worden gedaan voor mensen die een voorspellende test hebben gehad die aantoont dat ze een HD-genexpansie dragen, evenals voor mensen met risico die zichzelf niet willen laten testen.
Zoals alle keuzes is dit gecompliceerd. Het kind zal niet genetisch verwant zijn aan de ouder met risico, en er zal zorgvuldig moeten worden nagedacht over hoe en wanneer deze informatie met het kind te delen. Een ouder hoeft niet genetisch verwant te zijn aan hun kind om een volledige en liefdevolle ouderrol te vervullen. Er is veel ondersteuning beschikbaar voor mensen die deze weg kiezen, en dit kan worden besproken voordat besloten wordt om het proces te starten.
Veel stellen denken na over het adopteren van kinderen. Op veel plaatsen kunnen stellen waarvan één partner risico loopt op HD moeite hebben met het adopteren van een kind. Dit komt door de ziekte in de familie en het adoptiebureau moet ervoor zorgen dat het kind een stabiel thuis krijgt. Elk geval wordt echter individueel beoordeeld, dus het is de moeite waard om adoptie als optie te onderzoeken. Als je bent afgewezen voor adoptie, kunnen stellen met risico mogelijk pleegouders worden voor kinderen, omdat dit vaak een kortetermijnoptie is, waarbij je weken of maanden voor kinderen zorgt. De tijd die je doorbrengt met pleegkinderen, hoewel kort, kan vaak nog steeds een positieve impact hebben op het leven van het kind.
Toekomstige ontwikkelingen
Niet-invasieve prenatale diagnose is een nieuwere manier van testen tijdens de zwangerschap zonder een invasieve test uit te voeren, waardoor het kleine risico op een miskraam wordt vermeden. In plaats van een invasieve test die een monster neemt van de placenta of het vruchtwater, neemt NIPD een bloedmonster af van de ouder die zwanger is. Deze test zoekt naar kleine stukjes DNA van de foetus die in het bloed van de ouders circuleren.
NIPD kan plaatsvinden vanaf ongeveer 10 weken zwangerschap. NIPD vereist meestal enige voorbereiding door het laboratorium voorafgaand aan een zwangerschap. Het vereist monsters van het stel dat hun gezin wil uitbreiden en kan een monster van een aangedaan familielid vereisen.
NIPD is al beschikbaar in de kliniek voor sommige erfelijke aandoeningen en is in ontwikkeling voor HD, maar momenteel niet algemeen beschikbaar. Er zijn een aantal gevallen waarin NIPD niet geschikt zou zijn, bijvoorbeeld bij tweelingzwangerschappen. Als en wanneer NIPD voor HD beschikbaar komt, is het waarschijnlijk dat een resultaat dat aangeeft dat een zwangerschap risico loopt op HD, nog steeds zal worden gevolgd door een invasieve test om de testresultaten te bevestigen, voordat een zwangerschapsafbreking wordt gepland.
Hoe zit het met LHBTQIA+ mensen?
Alle hierboven besproken opties zijn waarschijnlijk beschikbaar voor LHBTQIA+ stellen met een familiegeschiedenis van HD die een gezin willen stichten. Er zou de extra stap zijn van het vinden van een sperma- of eiceldonor en indien nodig een draagmoeder, wat gepaard gaat met extra kosten en juridisch papierwerk.
In veel landen zal het LHBTQIA+ zijn je waarschijnlijk niet belemmeren om toegang te krijgen tot de gezinsplanningsoptie die het beste bij jou en je partner past. Er zal specifieke informatie zijn over de gezinsplanningstechnieken die in jouw land beschikbaar zijn voor LHBTQIA+ stellen die een gezin willen stichten.
Samenvatting
Er zijn een aantal opties beschikbaar voor mensen met risico op HD die een gezin willen stichten.
Niet iedereen kiest ervoor om genetische tests te ondergaan om een gezin te stichten, en dit is een volledig geldige optie.
Voor degenen die het risico willen wegnemen dat hun kind HD erft, hoeven ze mogelijk hun eigen risico op HD niet te kennen. Directe tests kunnen plaatsvinden wanneer we het resultaat van de ouder met risico kennen en is aangetoond dat ze de HD-genexpansie hebben. Terwijl exclusie- of niet-onthullingstests kunnen worden uitgevoerd voor stellen met risico die hun eigen testresultaten niet willen weten.
Directe en niet-onthullingstests kunnen plaatsvinden tijdens pre-implantatie genetische tests (PGT) waarbij embryo’s in het laboratorium worden gecreëerd en getest op hun risico op het ontwikkelen van HD, of een foetus kan worden getest tijdens de zwangerschap. Testen tijdens de zwangerschap kan invasief zijn via chorionvillusbiopsie (CVS) of niet-invasief (NIPD), maar beide zijn alleen opties voor degenen die zouden overwegen een zwangerschap met risico op het ontwikkelen van HD te beëindigen.
Er zijn andere opties beschikbaar voor stellen met risico, waaronder het gebruik van donor-eicellen/sperma of adoptie/pleegzorg van kinderen.
Deskundig advies, in de vorm van genetische counseling, zal je helpen de exacte opties te begrijpen die lokaal beschikbaar zijn en helpen onderzoeken welke optie voor jou goed voelt. De HD-vereniging in jouw land kan je vertellen hoe je in contact kunt komen met een genetisch counselor. Zoals bij zoveel dingen in het leven, is vooruitplannen en het begrijpen van alle opties van tevoren de sleutel.
Meer informatie
- Genetic Alliance (VK) pagina over pre-implantatie genetische tests
- National Society of Genetic Counselors (VS). Vind online een genetisch counselor. Je huisarts of regionale HD-vereniging kan je ook adviseren over doorverwijzing naar een genetisch counselor om vruchtbaarheidsopties te bespreken.
- De gids van de Human Fertility and Embryology Authority voor geassisteerde vruchtbaarheid voor mensen met genetische aandoeningen (VK)
Bronnen & Referenties
Voor meer informatie over ons openbaarmakingsbeleid, zie onze FAQ…


