Stamcellen en HD: verleden, heden en toekomst
Stamcellen – wie heeft ze nodig? Wetenschappers maken hersencellen van huidcellen. Kan dit HD helpen?

Let op: Automatische vertaling – Mogelijkheid van fouten
Om nieuws over HD-onderzoek en trial-updates zo snel mogelijk onder zoveel mogelijk mensen te verspreiden, is dit artikel automatisch vertaald door AI en nog niet beoordeeld door een menselijke redacteur. Hoewel we ernaar streven om nauwkeurige en toegankelijke informatie te verstrekken, kunnen AI-vertalingen grammaticale fouten, verkeerde interpretaties of onduidelijke formuleringen bevatten.Raadpleeg voor de meest betrouwbare informatie de originele Engelse versie of kom later terug voor de volledig door mensen bewerkte vertaling. Als je belangrijke problemen opmerkt of als je een moedertaalspreker van deze taal bent en wilt helpen met het verbeteren van nauwkeurige vertalingen, voel je dan vrij om contact op te nemen via editors@hdbuzz.net
Iedereen heeft wel eens van stamcellen gehoord, maar tot nu toe hebben stamcelbehandelingen voor de ziekte van Huntington teleurgesteld. Wetenschappers kunnen nu stamcellen maken van huidmonsters – en zelfs de tussenstap overslaan om direct hersencellen te maken. Stamcelbehandelingen zijn nog ver weg, maar deze cellen versnellen HD-onderzoek in het lab al wel.
Onvervangbare neuronen en atoombommen
De ziekte van Huntington is een neurodegeneratieve ziekte. Dat betekent dat de symptomen worden veroorzaakt door het afsterven van hersencellen die neuronen worden genoemd. Helaas voor HD-patiënten worden neuronen in de hersenen over het algemeen niet vervangen als ze eenmaal dood zijn.
Afbeelding: Annie Cavanagh, Wellcome Images
Hoe weten we dit? Lange tijd hadden wetenschappers aangenomen dat dit waar was, gebaseerd op studies bij dieren, maar het was moeilijk te bewijzen bij mensen. Maar in 2005 deden wetenschappers een opmerkelijk experiment waarbij ze straling van atoombommen gebruikten om aan te tonen dat neuronen in het menselijk brein meestal niet werden vervangen.
Van het midden van de jaren 1940 tot een wereldwijd teststopverdrag in 1963 werden honderden atoombommen tot ontploffing gebracht in de atmosfeer van de aarde. Deze bommen gaven grote hoeveelheden van een speciaal type koolstof vrij dat kan worden onderscheiden van natuurlijk voorkomende koolstof. Door de hoeveelheid van deze koolstof in neuronen te meten en te vergelijken met de hoeveelheid koolstof die wordt aangetroffen in bomen van een bekende leeftijd, konden wetenschappers de neuronen een ‘verjaardag’ toekennen.
De wetenschappers bepaalden dat neuronen in de hersenen verjaardagen hadden die heel dicht bij de werkelijke verjaardag van de persoon lagen waar ze bij hoorden. Dus over het algemeen zijn de neuronen die je hebt wanneer je sterft dezelfde als die je had toen je werd geboren. Dat is een van de redenen waarom neurodegeneratieve ziekten, zoals HD, zo schadelijk zijn – cellen die sterven worden niet vervangen.
Stamcellen en de droom van vervanging
Het feit dat neuronen zo belangrijk en zo onvervangbaar zijn, verklaart waarom veel mensen enthousiast zijn over stamcellen. Stamcellen zijn speciale cellen die het vermogen hebben om te veranderen in alle verschillende cellen waaruit een lichaam bestaat, van huidcellen tot levercellen tot hersencellen.
Elke levende persoon begon als een enkele cel – een bevruchte eicel. De cel deelde zich, en de nieuwe cellen werden alle verschillende soorten cellen in het lichaam. Het vermogen om te delen in cellen van verschillende typen wordt pluripotentie genoemd, en werd lange tijd beschouwd als een uniek kenmerk van stamcellen.
Stamcellen zijn heel moeilijk te verkrijgen. Historisch gezien was de enige plek waar wetenschappers wisten dat ze ze konden vinden de oorspronkelijke bron van alle cellen – het vroege stadium embryo. Een kleine massa cellen in het zich ontwikkelende embryo kon worden geïsoleerd en gekweekt in een laboratorium. Deze cellen zijn de ‘embryonale stamcellen’ die zoveel controverse en opwinding over de hele wereld hebben veroorzaakt. Embryonale stamcellen kunnen alleen worden verkregen uit afgebroken zwangerschappen, of de ongebruikte bevroren embryo’s van koppels die een vruchtbaarheidsbehandeling ondergaan.
Het unieke kenmerk van stamcellen om te veranderen in andere celtypen maakte ze heel belangrijk om te bestuderen, ondanks de moeilijkheid om ze te verkrijgen. De droom van veel mensen was dat als we konden begrijpen hoe cellen van het ene celtype in het andere veranderen, of ‘differentiëren’, we beschadigde weefsels zouden kunnen repareren. Als dit mogelijk zou zijn, zouden we stervende alvleesklier cellen kunnen vervangen en diabetes genezen, of breuken in het ruggenmerg repareren en beweging herstellen bij dwarslaesie patiënten. Op dezelfde manier hopen mensen dat we neuronen gemaakt van stamcellen zouden kunnen gebruiken om stervende neuronen in de hersenen van patiënten met ziekten zoals de ziekte van Huntington te vervangen.
De uitdaging van het vervangen van hersencellen
De taak van een neuron is om te ‘praten’ met andere neuronen met elektrische signalen. Die communicatie is de sleutel tot alle opmerkelijke dingen die hersenen doen. Bijvoorbeeld, de drang om je vinger te bewegen begint als een elektrisch signaal in een neuron in de hersenen nabij de bovenkant van je hoofd. Dit bereikt een neuron in je ruggenmerg, dat vervolgens een ander signaal helemaal naar de spieren van je vinger stuurt. Aan het einde van al deze signalering wordt een pufje chemicaliën vrijgegeven uit het uiteinde van het neuron dat begon in je ruggenmerg, waardoor een spier in je vinger samentrekt.
Je zult hebben gemerkt dat hier grote afstanden worden afgelegd. Slechts twee neuronen zijn direct betrokken bij deze beweging van de hersenen naar de punt van je vinger. Maar cellen zijn echt klein, nietwaar? Dus hoe bereiken ze zulke lange afstanden?
Neuronen groeien extreem lange uitsteeksels die axonen worden genoemd en die fungeren als elektrische draden om signalen te verzenden en ontvangen. Deze axonen kunnen extreem lang zijn: giraffen hebben axonen van wel 4,5 meter lang!
Om schade in de hersenen te repareren, moeten we nadenken over deze uitsteeksels, en alle verschillende verbindingen tussen neuronen, evenals de hersencellen zelf. Het repareren van de hersenen gaat niet alleen over het toevoegen van meer cellen – het moeilijke deel is het aansluiten van de cellen in de juiste patronen.
Een eenvoudige vingerbeweging behelst een paar cellen die in een lijn zijn verbonden. Maar sommige gespecialiseerde neuronen in de hersenen hebben honderdduizenden verbindingen met andere neuronen. Als je de verbindingen verkeerd maakt, kan het betekenen dat het hele netwerk niet correct zal functioneren.
Stamcelonderzoeken bij de ziekte van Huntington
In de hoop dat neuronen misschien zouden weten hoe ze zelf nieuwe verbindingen moeten groeien, hebben wetenschappers geprobeerd onrijpe menselijke neuronen, van embryoweefsel, direct in de zieke gebieden van de hersenen van patiënten met de ziekte van Huntington te injecteren.
Resultaten van deze onderzoeken waren gemengd. In een onderzoek waar vijf patiënten werden behandeld, vonden drie van hen dat hun symptomen stabiliseerden of zelfs verbeterden. Echter, de positieve resultaten hielden niet aan – de ziekte haalde hen in en ze begonnen weer achteruit te gaan.
“Het herstel van de hersenen gaat niet alleen om het toevoegen van meer cellen – het moeilijke deel is het op de juiste manier verbinden van de cellen.”
Waarom was de behandeling teleurstellend? Waarschijnlijk om verschillende redenen, waarvan de grootste was dat de cellen gewoon niet wisten welke verbindingen ze moesten maken. Maar daarbovenop waren de geïnjecteerde cellen niet altijd perfect gezond, en de HD-hersenen waar ze in werden geplaatst hadden ook al problemen, wat het moeilijk kon hebben gemaakt voor de cellen om te overleven. Bovendien waren de geïnjecteerde cellen genetisch verschillend van de hersenen waar ze in terechtkwamen, wat kan zorgen dat het immuunsysteem van de hersenen de cellen aanvalt of ‘afstoot’.
Op dit moment weten we gewoon niet hoe we nieuwe neuronen moeten vertellen hoe ze moeten verbinden en verbindingen moeten maken in volwassen hersenen. Maar vanwege deze moeilijkheden is het vervangen van cellen in de volwassen hersenen waarschijnlijk niet snel een wijdverspreide therapie voor HD.
Dus, zijn stamcellen nutteloos voor HD?
Deze moeilijkheden betekenen niet dat stamcellen irrelevant zijn bij HD.
Voor wetenschappers is een probleem zoals dit een uitdaging, en een kans om een mysterie op te lossen. We moeten werken met stamcellen om te proberen het probleem van het maken van de juiste verbindingen te begrijpen, met het langetermijndoel van het vervangen van cellen in de hersenen.
Met behulp van dieren kunnen we dit oefenen en proberen te leren over de mogelijkheden voor het opnieuw laten groeien van verbindingen tussen cellen. Op een dag zou dit werk kunnen leiden tot technologie die de veilige en nauwkeurige vervanging van cellen in de hersenen mogelijk maakt.
Maar ook al kunnen we stamcellen nog niet gebruiken om de ziekte van Huntington te behandelen, stamcellen zijn nu al belangrijk voor het helpen begrijpen en bestuderen van HD.
De uitdaging van het bestuderen van levende cellen
We hebben veel goede ideeën over hoe de HD-mutatie neuronen beschadigt, maar er zijn veel dingen die we nog steeds niet zeker weten. En het begrijpen van het probleem is een belangrijke stap op weg naar het oplossen ervan.
Maar het is echt moeilijk om laboratoriumonderzoek te doen naar menselijke neuronen. Levende menselijke hersencellen zijn heel moeilijk te verkrijgen – de meeste levende mensen gebruiken hun hersenen nog! En neuronen delen zich niet, dus wetenschappers kunnen niet eens een paar neuronen nemen en er grotere aantallen van kweken.
Zelfs als we een bron van volwassen menselijke neuronen hadden, zoals weefselmonsters van hersenoperaties, neuronen haten het om uit de hersenen te worden weggehaald en groeien niet goed in het lab.
We kunnen neuronen kweken die zijn genomen van jonge muizen of ratten, maar zelfs die zijn moeilijk in leven te houden. Belangrijk is dat we weten dat er enorme verschillen zijn tussen knaagdieren en mensen, vooral in de manier waarop hun hersencellen werken.
Vanwege deze moeilijkheden zijn veel van de cellen die worden gebruikt om de ziekte van Huntington in het lab te bestuderen tumorcellen die zijn genomen van verschillende kankers. Ze groeien goed in het lab en zijn gemakkelijk te hanteren. Het gebruik van deze cellen laat onderzoek sneller vooruitgaan, maar natuurlijk is HD geen kanker, en we zouden kunnen worden misleid door het bestuderen van cellen die zo verschillend zijn van de kwetsbare cellen bij HD.
Stamcellen als modellen van menselijke ziekten
Stamcellen kunnen worden aangemoedigd om te veranderen in elk type cel in het lichaam, door ze te behandelen met verschillende chemicaliën die ‘groeifactoren’ worden genoemd. We worden steeds beter in het begrijpen van de procedures en recepten voor het laten delen van stamcellen in verschillende celtypen.
In feite blijkt het veranderen van stamcellen in neuronen een van de gemakkelijkste dingen te zijn die je ermee kunt doen. Stamcellen lijken te ‘willen’ veranderen in neuronen. Neuronen gemaakt van stamcellen kunnen worden gebruikt om te proberen te begrijpen wat er misgaat bij de ziekte van Huntington, en om te proberen het te repareren.
Het is op dit gebied – basisonderzoek in het lab om te bestuderen wat er misgaat in cellen met de HD-mutatie – dat stamcellen het potentieel hebben, nu al, om HD-onderzoek te revolutioneren.
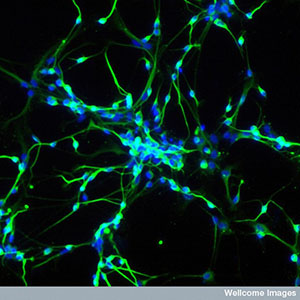
Afbeelding: Yirui Sun, Wellcome Images
Het bestuderen van HD in het type cellen dat sterft bij de ziekte maakt onderzoeksbevindingen veel geloofwaardiger – vooral wanneer de cellen van menselijke oorsprong zijn. Recentelijk zijn veel grote HD-labs begonnen met het werken met neuronen gemaakt van stamcellen om de ziekte beter te begrijpen.
En toen veranderde alles
Alles wat we weten over stamcellen veranderde in 2006. Twee Japanse onderzoekers, Kazutoshi Takahashi en Shinya Yamanaka, rapporteerden dat ze erin waren geslaagd gewone huidcellen om te zetten in stamcellen. Ze kwamen erachter hoe ze gewone cellen genomen van een huidmonster van een volwassen muis konden ‘herprogrammeren’ tot cellen die niet te onderscheiden waren van echte embryonale stamcellen. Ze noemden deze nieuwe cellen geïnduceerde pluripotente stamcellen of IPS-cellen.
Met die ene studie werd het idee dat stamcellen alleen van embryo’s konden worden verkregen in principe van de ene op de andere dag veranderd. Plotseling, in plaats van toekomstige behandelingen met stamcellen van embryo’s, konden we ons voorstellen dat we mensen zouden behandelen met stamcellen gemaakt van hun eigen lichaam – met hun eigen DNA.
Natuurlijk zou, wat stamcelbehandeling betreft, het probleem van het laten maken van de juiste verbindingen door de cel er nog steeds zijn. Maar IPS-cellen zouden tenminste de problemen van voorraad en het genetische verschil tussen de geïnjecteerde cellen en de hersenen kunnen oplossen.
Toen veranderde het weer
Net toen wetenschappers gewend raakten aan het idee dat stamcellen misschien veel gemakkelijker te verkrijgen zouden zijn dan ze ooit hadden voorgesteld, veranderde alles weer. In 2010 deed een groep onderzoekers aan Stanford University iets misschien nog opmerkelijkers.
In plaats van te beginnen met volwassen cellen, ze om te zetten in stamcellen en die stamcellen vervolgens om te zetten in een ander celtype, besloten ze de tussenstap over te slaan.
Ze toonden aan dat ze huidcellen direct konden omzetten in neuronen. Beginnend met een huidmonster konden ze cellen in een schaaltje kweken, een cocktail van chemicaliën en genen toevoegen om ze te herprogrammeren, en de huidcellen zouden veranderen in neuronen – die onvervangbare hersencellen waarvan het verlies ten grondslag ligt aan zoveel ziekten, waaronder HD.
Wetenschappers hebben decennia lang gedacht dat zodra een cel zich ‘vastlegt’ op het ene of andere type, die beslissing niet kan worden veranderd. Duidelijk is die basisaanname verkeerd.
Cellen omzetten en HD
Deze opmerkelijke vooruitgang – het vermogen om pluripotente stamcellen te maken van volwassen patiënten, en het vermogen om volwassen cellen direct te herprogrammeren – hebben het landschap van de biologie getransformeerd.
Dingen die vijf jaar geleden als sciencefiction leken, zijn plotseling mogelijk. Wat de toekomst ook brengt, wetenschappers kunnen nu minimaal neurodegeneratieve ziekten bestuderen in menselijke neuronen, gekweekt van echte menselijke patiënten.
Maar zelfs met deze nieuwe bronnen van neuronen blijven we zitten met het probleem dat het simpelweg injecteren ervan in de hersenen van volwassenen waarschijnlijk niet effectief neuronen zal vervangen die sterven bij ziekte. We moeten een manier vinden om de juiste verbindingen tussen hen opnieuw te laten groeien, die cruciaal zijn voor het juiste functioneren van de hersenen. Dat is iets waar onderzoekers van de ziekte van Huntington aan werken, en het is dichterbij dan ooit – maar nog steeds ver weg.
Ondertussen begint de IPS-celrevolutie net door te werken in ons begrip van de ziekte van Huntington. Naarmate de technieken meer gevestigd raken, zullen IPS-cellen cruciale hulpmiddelen worden in de zoektocht naar effectieve behandelingen.
Meer informatie
Voor meer informatie over ons openbaarmakingsbeleid, zie onze FAQ…


