
De ziekte van Huntington therapeutische conferentie 2018 – Dag 2
DNA in de spotlights op dag 2 van de ziekte van Huntington Therapeutische Conferentie in Palm Springs

Updates van dag 2 van de ziekte van Huntington Therapeutische Conferentie gericht op DNA-herstel bij de ZvH.
Woensdagochtend – DNA-herstel bij de ZvH
Goedemorgen vanaf de ziekte van Huntington Therapeutische Conferentie 2018! De update van vandaag is relatief kort omdat de middag was gericht op posterpresentaties. De ochtendsessie was gericht op de rol van DNA-reparatie bij de ZvH – tegenwoordig een hot topic dankzij zeer interessante genetische studies van ZvH-patiënten. Deze enorme studies toonden aan dat genetische variaties, buiten het ZvH-gen, bijdragen aan hoe snel ZvH-symptomen optreden bij mensen die deze genetische variaties hebben. Verrassend genoeg zaten veel van deze variaties in genen die cellen helpen DNA te herstellen.

Als eerste brengt Jong-Min Lee, van Massachusetts General Hospital, de menigte op de hoogte van de nieuwste resultaten van het GeM-HD-consortium – de internationale groep onderzoekers die genetische variaties zoeken die het ontstaan van de ZvH beïnvloeden. Het GeM-HD-consortium gebruikt microchips die kleine genetische variaties aflezen over het hele genoom van duizenden ZvH-patiënten. Deze enorme dataset stelt hen in staat om de vraag te stellen: beïnvloeden deze variaties hoe vroeg of laat de ZvH optreedt? De nieuwste versie van de GeM-HD-analyse omvat 9.000 ZvH-patiënten! Door deze grotere steekproefomvang konden ze nog meer variaties identificeren die het begin van de ZvH moduleren. Deze variaties liggen opvallend dicht bij nog meer DNA-herstelgenen. Lee beschrijft een zeer subtiele variatie in de sequentie van het ZvH-gen zelf die ook van invloed is op wanneer de ZvH-symptomen beginnen. Het meest dramatische effect dat GeM-HD heeft waargenomen, betreft een gen genaamd FAN1. Sommige variaties in dit gen hebben een gunstig effect op het begin van de ZvH en andere variaties hebben hier een slecht effect op. Dit suggereert dat iets dat FAN1 doet centraal staat in de progressie van de ZvH. Lee levert nog meer bewijs dat suggereert dat bij mensen met meer Fan1 in hun hersenen, de ZvH later begint. Dit toont de kracht van het doen van genetische studies aan – als we een manier kunnen vinden om de activiteit van Fan1 te versterken, lijkt het waarschijnlijk dat dit gunstig zou zijn voor de progressie van de ZvH.
Guo-Min Li, van de University of Texas Southwestern, bestudeert een proces genaamd ‘mismatch repair’, een van de manieren waarop cellen bepaalde soorten DNA-schade herstellen. Mismatch-reparatie stelt cellen in staat om kleine fouten op te lossen die opduiken wanneer cellen hun DNA kopiëren. Mutaties in deze genen leiden tot hoge kankercijfers, omdat genetische fouten niet worden gecorrigeerd. Li herinnert het publiek eraan dat, hoewel herstel van verkeerde combinaties normaal gesproken erg nuttig is voor cellen om gezond te blijven, het soms fouten maakt. Eén daarvan is de neiging tot verlenging van lange herhalende stukken DNA. De mutatie die elk geval van de ZvH veroorzaakt – een stuk van de DNA-letters ‘C-A-G’ – is een van deze herhalende stukjes DNA. Het laboratorium van Li onderzoekt het proces waardoor herstel van lange stukken CAG door mismatch-reparaties langer wordt. Li’s lab heeft een aantal specifieke herstelprocessen voor verkeerde combinaties geïdentificeerd die CAG-uitbreidingen stimuleren – hij suggereert dat ze een goed doelwit kunnen zijn voor nieuwe ZvH-behandelingen.
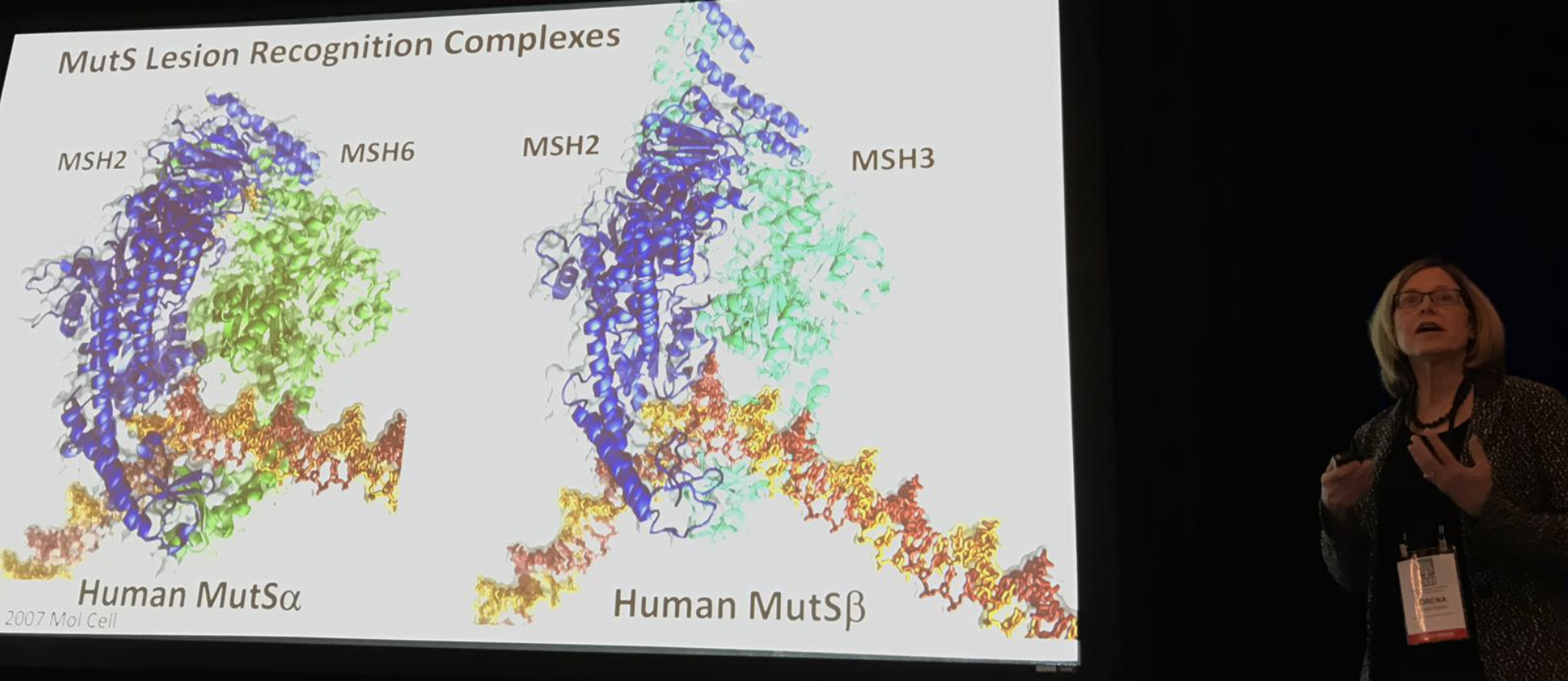
Lorena Beese, van Duke, bestudeert ook mismatch-reparatie. Haar lab richt zich op de precieze manieren waarop de mismatch-reparatie-eiwitten hun werk uitvoeren – fouten herkennen, deze eruit knippen en vervolgens het DNA weer aan elkaar naaien. De machines die het laboratorium van Beese in detail heeft beschreven, kunnen toekomstige doelen zijn voor geneesmiddelen die zijn ontworpen om de interactie met lange CAG-kanalen te veranderen, zoals die in het ZvH-gen.
Peter McKinnon, van St. Jude Children’s Research Hospital, is een expert op het gebied van DNA-herstel in de hersenen. Hij spreekt de conferentie toe over de specifieke soorten DNA-schade die in de hersenen voorkomen. De hersenen zijn interessant vanuit het oogpunt van DNA-reparatie, omdat de neuronen in onze hersenen gedurende het grootste deel van ons leven niet delen. Dit betekent dat ze sommige mogelijkheden van de DNA-herstelroutes niet kunnen gebruiken die alleen werken bij cellen die zichzelf delen. Het laboratorium van McKinnon bestudeert een specifiek soort DNA-schade genaamd ‘base excision repair’, een proces voor het herstellen van schade aan slechts één van de twee DNA-strengen.
Partha Sarkar van de Universiteit van Texas bestudeert het huntingtine-eiwit en de directe interacties met DNA en DNA-hanterende eiwitten. Het blijkt dat mutant huntingtine rondhangt met een eiwit genaamd PNKP, wiens taak het is om voor DNA te zorgen. Hierdoor voorkomt het dat het zijn werk doet. Dit verhoogt de mogelijkheid dat de ZvH-mutatie DNA-schade versnelt.
Voor meer informatie over ons openbaarmakingsbeleid, zie onze FAQ…


