Astrocyten: de nieuwe ster in het huntingtononderzoek?
Een nieuw artikel vat samen wat het huntington-onderzoeksveld gevonden heeft over astrocyten. Deze stervormige cellen helpen de hersencellen gezond te houden en kunnen worden gebruikt voor de ontwikkeling van huntingtontherapieën.
Geschreven door Dr Sarah Hernandez 2 november 2023 Bewerkt door Dr Leora Fox Vertaald door Gerda De Coster Origineel gepubliceerd op 19 april 2023
De meest voor de hand liggende veranderingen met betrekking tot de ziekte van Huntington (ZvH) vinden plaats in neuronen, de boodschappercellen van het zenuwstelsel die informatie verzenden en ontvangen doorheen de hersenen en het ruggenmerg. Verschillende andere celtypen worden echter ook beïnvloed door de ZvH. Een recent gepubliceerd artikel besprak onderzoeksresultaten van verschillende laboratoria en beschrijft hoe een specifiek type hersencel, astrocyt genaamd, bijdraagt aan de ZvH. Dit overzichtsartikel beschrijft waarom onderzoekers aandacht moeten besteden aan meer dan alleen de neuronen om effectieve behandelingen voor de ziekte te ontwikkelen. Laten we uitzoeken waarom!
De hersenen – meer dan neuronen
Het huntingtine-gen wordt in elke cel van ons lichaam aangetroffen. Dat betekent dat het toegenomen aantal CAG-herhalingen binnen het huntingtine-gen - waardoor de ZvH wordt veroorzaakt - ook in elke cel wordt aangetroffen. Maar sommige organen, zoals de hersenen, zijn gevoeliger voor schade door het mutante huntingtine (HTT). In de hersenen zijn er bepaalde gebieden die bijzonder kwetsbaar zijn gebleken bij de ZvH, zoals het striatum – een gebied dat zich in het centrum van de hersenen bevindt en helpt bij het controleren van zaken zoals besluitvorming en vrijwillige bewegingen.
Het striatum bestaat uit verschillende celtypen, waaronder neuronen, waarover we veel horen bij de ZvH. Neuronen zijn de boomvormige cellen die elektrische signalen doorgeven waardoor we kunnen denken, voelen en bewegen. Ze zijn toevallig ook het celtype dat het meest wordt aangetast bij de ziekte en verliezen hun vermogen om te functioneren naarmate de ziekte voortschrijdt. Maar het meest voorkomende celtype in het striatum zijn niet de neuronen maar een celtype genaamd glia.
Glia zijn ondersteunende cellen die helpen om de hersenen gezond te houden. Er zijn verschillende soorten gliacellen en recenter bewijs op het gebied van de ZvH heeft ons geleerd dat deze verschillende celtypen ook een rol spelen bij de ziekte. Begrijpen hoe ze bijdragen aan de ZvH en hoe ze tijdens de ziekte worden beïnvloed, kan helpen bij het ontwikkelen van nieuwe therapieën.
Astrocyten in de schijnwerpers
Een bepaald type gliacellen dat de laatste tijd veel aandacht heeft gekregen in het huntingtononderzoek, is een celtype dat astrocyten wordt genoemd. Dit zijn stervormige cellen die de neuronen ondersteunen en ervoor zorgen dat ze een fijne omgeving hebben waarin ze kunnen gedijen – ze houden de chemicaliën rond de neuronen in evenwicht, leveren voedingsstoffen en beschermen ze. Een motto van astrocyten is: “gelukkige neuronen, gezond brein”!
“Een motto van astrocyten is: gelukkige neuronen, gezond brein! ”
Er zijn veel astrocyten nodig om ervoor te zorgen dat neuronen in de hersenen gelukkig en gezond blijven. Ongeveer 20-40% van de hersenen bestaat uit astrocyten! In tegenstelling tot neuronen blijven astrocyten zich gedurende hun hele leven vermenigvuldigen. Ook in tegenstelling tot neuronen sterven astrocyten niet in grote aantallen tijdens het verloop van de ZvH, maar ze lijken wel te veranderen. Aangenomen wordt dat deze veranderingen impact hebben op hun vermogen om neuronen te ondersteunen en gezond te houden. Uiteindelijk kunnen die veranderingen bijdragen aan de unieke kwetsbaarheid van neuronen bij de ziekte.
Om samen te vatten wat het huntington-veld heeft geleerd over astrocyten, werkten Dr. Baljit Khakh van de University of California, Los Angeles en Dr. Steve Goldman van de University of Rochester samen om een uitgebreid overzicht te schrijven over de wetenschappelijke bevindingen van de afgelopen 10 jaar op dit gebied. Drs. Khakh en Goldman zijn beide experten op het gebied van neurodegeneratieve ziekten en hebben hun loopbaan grotendeels gericht op het bestuderen van gliacellen en astrocyten. Hun overzicht omvatte wat we weten over astrocyten uit menselijke hersenen en muismodellen, en ze suggereerden hoe we deze informatie kunnen gebruiken om therapieën te ontwikkelen.
De kip of het ei
Weefselmonsters van mensen die genereus hun hersenen hebben gedoneerd voor onderzoek, hebben bijgedragen aan ons begrip over astrocyten. Deze kostbare stalen hebben ons geleerd dat astrocyten in huntingtonhersenen van vorm veranderen en de moleculaire ‘labels’ verliezen die bijdragen aan hun unieke identiteit. Deze veranderingen nemen toe naarmate de ziekte vordert en men denkt dat hun vermogen om goed te functioneren hierdoor vermindert. In menselijke hersenen is het echter niet duidelijk of veranderingen in de astrocyten de oorzaak of het gevolg zijn van de kwetsbaarheid van neuronen bij huntington.
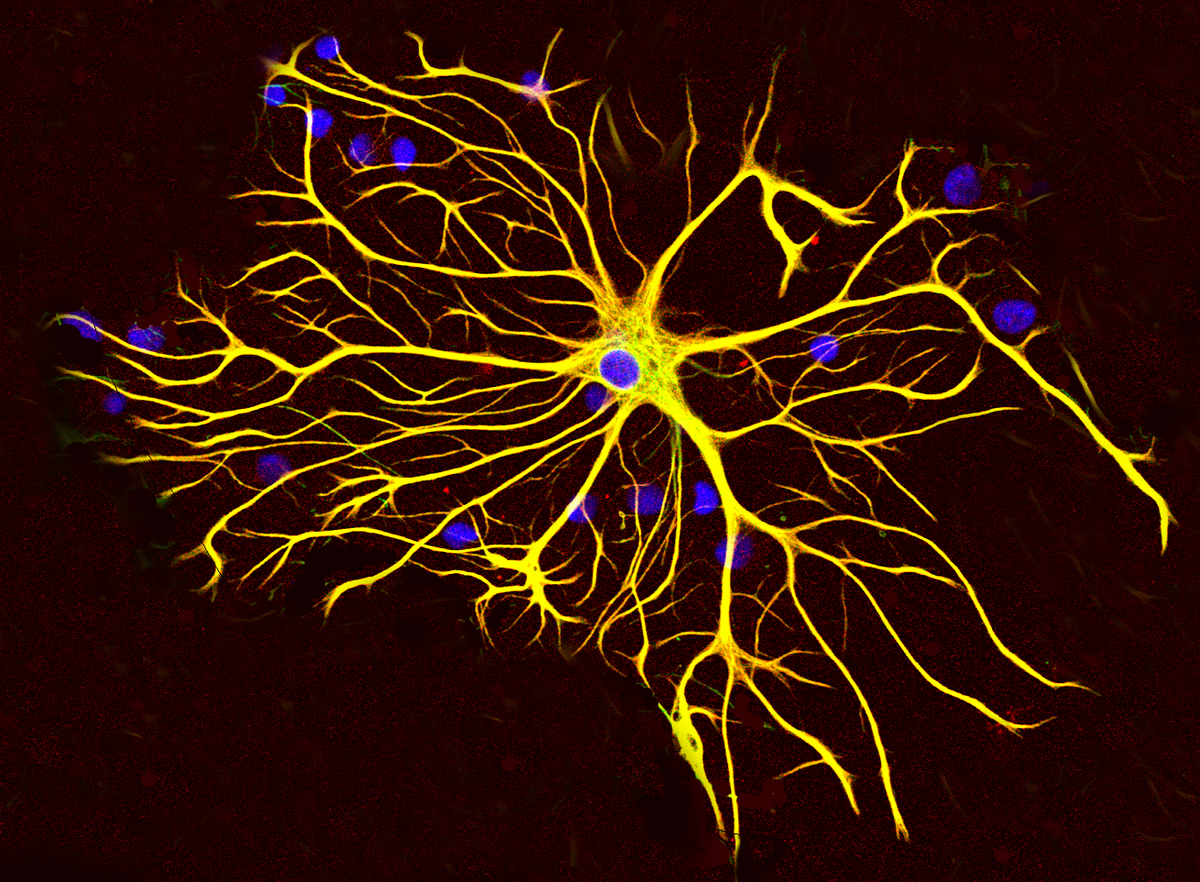
Om oorzaak en gevolg tussen astrocyten en neuronen in de ziekte te begrijpen, wenden wetenschappers zich tot diermodellen. Op basis van deze modellen kunnen onderzoekers ingewikkelde biologische vragen stellen en antwoorden krijgen. Dit zou niet mogelijk zijn met menselijk weefsel.
Astrocyten - zowel oorzaak als gevolg
Toen ze keken naar de vorm en de functie van astrocyten in huntingtonmuizen, ontdekten onderzoekers veranderingen vergelijkbaar met wat ze zagen in menselijke hersenen. Ze ontdekten ook dat veranderingen in de vorm van de astrocyten werden waargenomen voordat neuronen het vermogen verloren om te communiceren. Bovendien merkten de onderzoekers veranderingen op in de kalium- en calciumspiegels geproduceerd door de astrocyten. Neuronen gebruiken deze elementen om met de hersenen en het lichaam te communiceren. Deze bevindingen zouden kunnen suggereren dat de ZvH leidt tot veranderingen in astrocyten die de afbraak van neuronen veroorzaken .
Met behulp van genetische manipulatietechnieken bij muizen verlaagden onderzoekers enkel de mutante kopie van HTT in de astrocyten of in de neuronen. Met deze techniek konden ze uitzoeken welk celtype de specifieke gevolgen van de ZvH veroorzaakt. Best een slimme tactiek! Ze ontdekten dat symptomen van huntington bij muizen, zoals gedragsveranderingen, voornamelijk afkomstig zijn van neuronen en dat die veranderingen in de neuronen de functie van astrocyten verstoort.
“De auteurs suggereren dat de meest effectieve therapeutische strategieën waarschijnlijk een tweeledige aanpak vereisen: het verlagen van het mutante HTT in de neuronen terwijl het vermogen van astrocyten wordt hersteld om een ondersteunende omgeving in de hersenen te creëren. ”
Deze resultaten lijken echter een hoofdbreker te zijn - wat komt eerst en wat beïnvloedt het ander. Het is een beetje een kip-en-ei-scenario. Hoewel het niet helemaal duidelijk is of astrocyten of neuronen de oorzaak of het gevolg zijn, is het duidelijk dat beide celtypen bijdragen aan bepaalde symptomen van de ZvH en worden beïnvloed door de ZvH.
Een andere groep onderzoekers verving de cellen om de rol van astrocyten bij de ZvH te onderzoeken. Ze transplanteerden niet-huntingtonastrocyten in een muis met de ziekte en ontdekten dat de muizen minder symptomen hadden en langer leefden. Ze deden ook het omgekeerde experiment door huntingtonastrocyten te transplanteren in een niet-huntingtonmuis en ontdekten dat die muizen huntingtonsymptomen ontwikkelden. Deze bevindingen suggereren dat sommige huntingtonsymptomen in ieder geval worden veroorzaakt door astrocyten en dat het vervangen van zieke astrocyten een benadering zou kunnen zijn om de huntingtonsymptomen te verminderen.
Samen werken aan effectieve behandelingen
De onderzoeken die in dit overzichtsartikel aan bod komen suggereren dat diermodellen nauwkeurig ziekteveranderingen nabootsen die worden waargenomen in de astrocytes bij mensen Van deze dieren hebben we geleerd dat neuronen de belangrijkste aanjagers lijken te zijn van huntingtonsymptomen. Astrocyten zelf kunnen echter ook huntingtonveranderingen veroorzaken en hun verminderde functie in de ZvH verstoort de neuronen nog verder.

De auteurs suggereren dat de meest effectieve therapeutische strategieën waarschijnlijk een tweeledige aanpak vereisen: het verlagen van mutant HTT in neuronen terwijl het vermogen van astrocyten wordt hersteld om een ondersteunende omgeving in de hersenen te creëren. Dus hoewel we misschien vaker horen over bepaalde therapeutische strategieën, zoals huntingtineverlaging, benaderen wetenschappers over de hele wereld therapieën vanuit verschillende invalshoeken.
Het werk in het veld is aan de gang om de bijdrage van astrocyten aan de ZvH volledig te begrijpen. Tot nu toe hebben onderzoekers echter aangetoond dat zowel neuronen als astrocyten worden beïnvloed door de ziekte. De celtypen werken samen en inzicht in hoe elk door de ander wordt beïnvloed, kan leiden tot de ontwikkeling van effectieve therapeutische strategieën.


