Het brein bij de ZvH: groter dan de som van zijn delen?
Een belangrijke nieuwe studie stelt de vraag: welke delen van het brein hebben de meeste hulp nodig bij de ZvH?
 Geschreven door Dr Jeff Carroll 9 januari 2015 Bewerkt door Professor Ed Wild Vertaald door Gerda De Coster Origineel gepubliceerd op 19 mei 2014
Geschreven door Dr Jeff Carroll 9 januari 2015 Bewerkt door Professor Ed Wild Vertaald door Gerda De Coster Origineel gepubliceerd op 19 mei 2014
De symptomen van de ZvH worden veroorzaakt door beschadiging van de hersenen, maar niet alle delen van de hersenen worden in gelijke mate getroffen. Dit roept een belangrijke vraag op; als we een behandeling zouden hebben die slechts een klein deel van de hersenen kan helpen, welk gedeelte zouden we dan kiezen? Een nieuwe studie met muizen van William Yang aan UCLA (University van California in Los Angeles) tracht deze vraag te beantwoorden.
Welke gebieden in de hersenen veroorzaken de ZvH?
De belangrijkste symptomen van de ziekte van Huntington zijn bekend bij de meeste familieleden: achteruitgang van het denkvermogen, toename van emotionele problemen en bewegingsstoornissen. Wetenschappers geloven dat deze problemen allemaal hun oorsprong vinden in de verstoring èn het verlies van hersencellen.
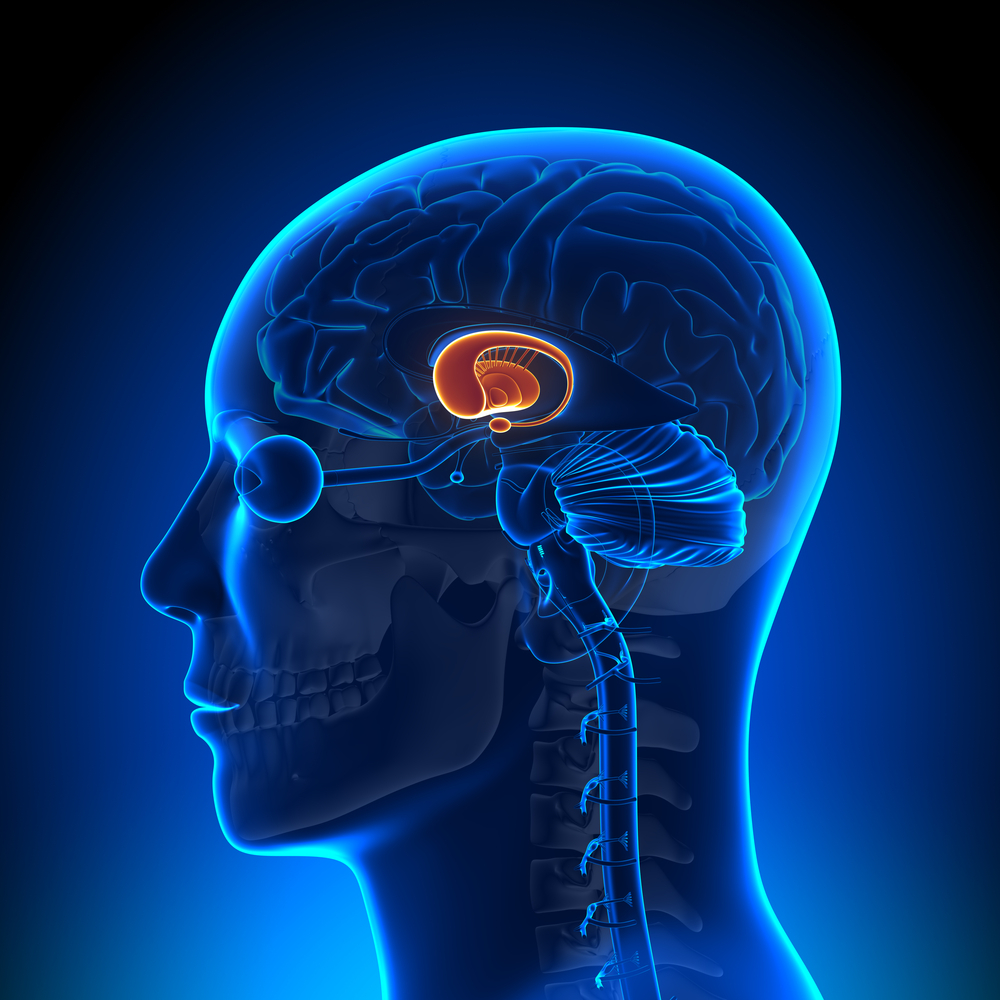
Maar niet zomaar overal in de hersenen. Het patroon van celverlies bij de ZvH is zeer specifiek. Op basis van de hersenen kan een bekwame arts je vertellen wie overleden is aan de ZvH, de ziekte van Alzheimer of de ziekte Parkinson. Hij kan dit onderscheid maken omdat bij elk van deze ziektes sommige delen van de hersenen prominenter aangetast zijn dan andere.
Het striatum is het meest kwetsbare deel van de hersenen bij de ZvH. Het striatum is een relatief kleine structuur, aan de onderkant van de rimpelige buitenkant van de hersenen, die de cortex wordt genoemd.
Tijdens het verloop van de ZvH zullen cellen in het striatum zowel als in de cortex krimpen, slechter gaan functioneren en uiteindelijk afsterven. Onderzoek na onderzoek waaraan vele honderden vrijwilligers deelnamen, heeft uitgewezen dat het striatum de eerste plaats is in de hersenen die krimpt, bij mensen met de de ZvH mutatie.
Hersenconnectiviteit
In veel opzichten is het brein een uniek orgaan in vergelijking met andere organen in je lichaam. Eén manier waarin het brein uniek is, is dat de cellen die ons helpen met denken (neuronen) sterk met elkaar verbonden zijn. Gemiddeld is elk van de 100 miljard neuronen in de hersenen verbonden met duizenden andere neuronen - waardoor elk menselijk brein wel 100 triljoen verbindingen heeft!
De verbindingen in de hersenen zijn niet willekeurig: specifieke delen van de hersenen weten dat het hun taak is om met elkaar praten. Je wil er zeker van zijn dat de optische zenuw die uit de achterkant van je oog komt, goed is aangesloten op het deel van de cortex dat verantwoordelijk is voor het gezicht bijvoorbeeld.
Zo zijn het striatum en de cortex ook zeer nauw verbonden. Misschien stuurt de cortex wel miljoenen verbindingen naar het striatum. Interessant is dat de verbindingen niet in twee richtingen hoeven te gaan - het striatum stuurt zijn eigen verbindingen naar ergens anders in de hersenen.
Verbonden zijn is niet enkel de manier waarop neuronen met elkaar communiceren: het is de manier waarop ze in leven blijven! Wetenschappers weten al vele jaren dat neuronen die beroofd worden van hun verbindingen met andere neuronen, daadwerkelijk zullen sterven!
“Is de behandeling van het striatum voldoende? Het antwoord, gebaseerd op de beste informatie die we tot nu toe hebben is, waarschijnlijk niet. ”
Dit roept interessante vragen op bij de ZvH. Welk weefsel is verantwoordelijk voor welke specifieke symptomen van de ZvH aangezien zowel de cortex als het striatum lijken te krimpen? Leidt verlies in het striatum (het diepe deel van het circuit) tot verlies in de cortex, of vice versa?
Muizentrucjes
Dit soort vragen kunnen niet worden beantwoord in mensen maar we kunnen muizen gebruiken om tot op het bot uit te zoeken wat er gebeurt in hersenen met de ziekte van Huntington. Een team van wetenschappers onder leiding van William Yang (UCLA) maakte gebruik van een speciaal soort ZvH-muizen om te proberen deze kwestie te begrijpen.
De muizen die William gebruikte, zijn genetisch gemanipuleerd zodat ze het mutante ZvH gen hebben (normale muizen krijgen nooit ZvH). Tevens kunnen wetenschappers bepalen in welke delen van de hersenen het mutante gen uitgeschakeld kan worden.
Dit geeft ons de mogelijkheid om drie verschillende soorten van huntingtonmuizen te vergelijken: ‘gewone’ ZvH muizen die overal in de hersenen abnormale activiteit hebben, ZvH muizen zonder het mutante gen in het striatum en ZvH muizen zonder het mutante gen in de cortex. Door deze groepen te vergelijken, kunnen we proberen te begrijpen welk hersengebied het meest verantwoordelijk is voor de symptomen van de ziekte, althans in dit muismodel.
Bevindingen
De groep van Yang gebruikte een aantal laboratoriumproeven om het muisgedrag, waarvan we weten dat het verandert in huntingtonmuizen, te meten. Bij deze proeven presteren de huntingtonmuizen zoals verwacht, slechter dan de normale muizen.
Gezien het feit dat het striatum het meest getroffen gedeelte van de hersenen is bij ZvH patiënten, zouden we verwachten dat het elimineren van het mutant ZvH gen op die plaats het meeste voordeel voor de muizen zou hebben. Eliminatie van het mutante ZvH gen in het striatum leidde wel tot enige verbetering in het gedrag, maar het verschil was te klein om er zeker van te zijn.

Verrassend was dat muizen die geen gemuteerd ZvH gen in de cortex hebben ( bij mensen wordt de cortex pas later getroffen) het beter leken te doen dan muizen die geen ZvH gen in het striatum hebben. Dit suggereert dat de cortex echt belangrijk is bij de ziekte van Huntington.
Iets gelijkaardig was te zien wanneer het team de veranderingen in de fysieke structuur van de hersenen bekeek. ZvH muizen zonder het mutante gen in hun cortex zagen er beter dan ZvH muizen zonder het mutante gen in het striatum.
Tenslotte merkte het team van Yang op dat het nodig was om het ZvH gen uit te schakelen zowel in de cortex als in het striatum om alle symptomen van de ziekte te voorkomen.
Implicaties
Dit onderzoek suggereert dat het mutante Huntington eiwit problemen veroorzaakt in de cortex en het striatum en dat beide gebieden van belang zijn.
Eender welke therapie die zich alleen op het striatum richt, kan enkel een beperkt effect hebben, gezien de resterende problemen elders in de hersenen. Dit is niet alleen een academische kwestie. Bepaalde voorgestelde therapieën voor de ZvH, met inbegrip van sommige vormen van gentherapie en stamcelvervanging, zullen zich waarschijnlijk enkel richten op het striatum.
Dit werk is gebaseerd op genetische trucjes die niet mogelijk zijn bij mensen, zodat het niet onmiddellijk verwijst naar een therapie voor mensen. Maar het wordt gebruikt om een antwoord te vinden op een vraag waar ZvH wetenschappers al lang over redetwisten: ‘is een behandeling van het striatum genoeg?’. Het antwoord, gebaseerd op de beste gegevens die we hebben tot nu toe is ‘waarschijnlijk niet’.
Waarom zijn we dan zo enthousiast over dit nieuwe werk? Omdat we deze lessen liever leren in muizen en ze gebruiken om de best mogelijke studies op te zetten voor mensen met de ZvH. Dit werk is een belangrijk stukje van de puzzel en hopelijk zal het ons in de toekomst helpen om de best mogelijke klinische proeven te ontwerpen.


